Термообработка сталей в ООО КВАДРО
Наше предприятие уже почти четверть века производит на заказ термообработку металлов в Санкт-Петербурге. Заказать термообработку у нас Вы можете, оставив Вашу заявку на электронной почте или позвонив нам.
Мы производим термообработку сталей (в т.ч. нержавеющих, инструментальных и т.п.)по чертежам Заказчика или заданным режимам, а так же иных металлов и сплавов (алюминиевых и титановых, латуней и бронз, и т.д.).
Основные виды термической обработки металлов, осуществляемые на нашем предприятии на заказ:
-
закалка (в т.ч. в соляных ваннах, например, для калки быстрорезов);
-
отпуск;
-
отжиг;
-
нормализация;
-
улучшение;
Напоминаем так же, что у нас вы можете воспользоваться широким спектром методов металлообработки, включая фрезерные работы и токарную обработку.

Цементит: формы существования
Так называют соединение углерода и железа. Это компонент чугуна и некоторых сталей. В него входит 6,67% углерода.
В его кристалл входит несколько октаэдров, они расположены друг по отношению к другу с некоторым углом. Внутри каждого из них расположен атом углерода. В результате такого построения получается следующая картина – один атом вступает в связь с несколькими атомами железа, а железо в свою очередь связано с тремя атомами этого элемента.
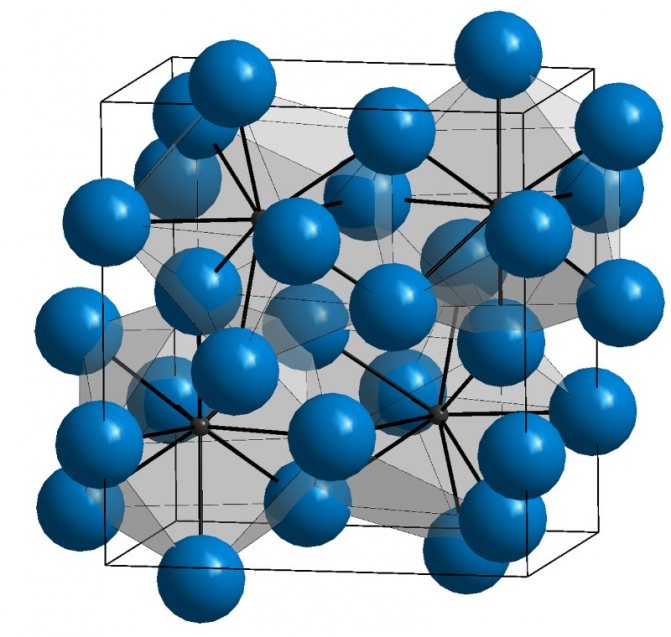
Кристаллическая решетка цементита
У этого вещества имеются все свойства, которые присущи металлам – электропроводность, своеобразным блеском, высокая теплопроводность. То есть, смесь железа и углерода, ведет себя как металл. Этот материал обладает определенной хрупкостью. Большая часть его свойств определена сложным строением кристаллической решетки.
Этот материал плавится при 1600 градусах Цельсия. Но на этот счет существует несколько мнений, одни исследователи считают, что его температура плавления лежит в диапазоне от 1200 до 1450, другие определяют, что верхний уровень равен 1300 °С.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.
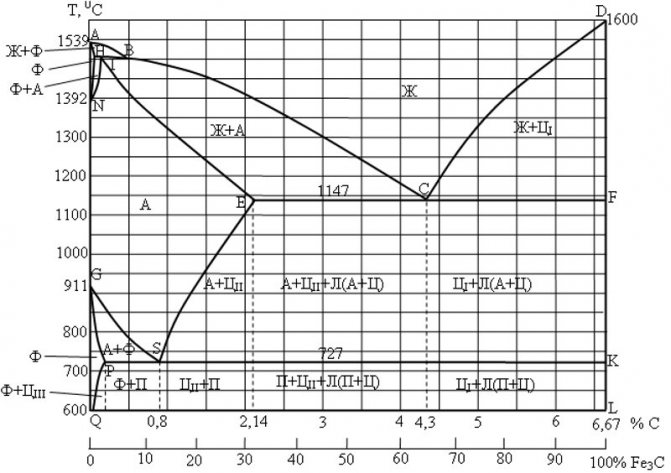
Диаграмма железо-цементит
Первичный, получается из жидкости при закалке сплавов, которые содержат в себе 5,5% углерода. Первичный имеет форму в виде крупных пластин.
Вторичный
Этот элемент получается из аустенита при охлаждении последнего. На диаграмме этот процесс этот процесс можно видеть по диаграмме Fe – C. Цементит представлен в виде сетки, размещенной по границам зерен.
Третичный
Этот тип, является производным от феррита. Он имеет форму иголок.
В металлургии существуют и другие формы цементита, например, цементит Стеда и пр.
Другие структурные составляющие в системе железо углерод
Перлит
Перлит – это механическая смесь, которая состоит из феррита и цементита. Ледебурит представляет собой переменный раствор.

Перлит
При температуре от 1130 и до 723 °С в его состав входят аустенит и цементит. При более низких температурах он состоит из аустенит заменяет феррит.
ЦЕМЕНТИТ
ЦЕМЕНТИТ
– химическое соединение (карбид железа) в железоуглеродистых сплавах, и соответствующее максимальному содержанию углерода. Химическая формула цементита Fe3C, концентрация углерода – 6,67% (по массе) (по массе). Также по теме: УГЛЕРОД
Как следует из диаграммы состояния железо – углерод, как фазовая составляющая цементит есть в железоуглеродистых сплавах уже при очень малых содержаниях углерода (сотые доли процента) и его количество возрастает по мере увеличения содержания углерода. При этом цементит входит в структурную составляющую перлит (смесь феррита и цементита), существующую в стали, наряду с ферритом. По мере увеличения содержания углерода доля перлита в структуре возрастает и, соответственно, возрастает количество цементита. При содержании углерода 0,8% (эвтектоидная сталь) структура целиком состоит из перлита. При дальнейшем увеличении содержания углерода в стали, кроме перлита появляется избыточный цементит. Вплоть до содержания углерода 1,7% железоуглеродистые сплавы называются сталями, при более высоких концентрациях до максимальной 6,67% – чугунами.
В процессе термической обработки в сталях цементит образуется при охлаждении и распаде твердого раствора (аустенита), в чугунах – непосредственно при охлаждении из жидкого состояния. Соответствующая структурная составляющая из цементита и аустенита, называется ледебурит с общим содержанием углерода в 4,3%. При дальнейшем увеличении доли углерода при охлаждении из жидкости при охлаждении выделяются цементит (первичный) и ледебурит. В чугунах, содержащих аустенит, при охлаждении происходит перлитное превращение, также приводящее к выделению цементита.
Также по теме:
ХИМИЯ
Цементит имеет высокую твердость и хрупкость, поэтому железоуглеродистые сплавы, содержащие много цементита, не поддаются пластической деформации.
Из-за различных механизмов образования цементита его микроструктура может очень сильно отличаться для сплавов с различным содержанием углерода после различных термических обработок и размеры кристаллов могут меняться от сотых долей до нескольких мм.
Кристаллическая структура цементита, определенная рентгеноструктурным анализом, – ромбическая. Ее элементарная ячейка, т.е. минимальная конфигурация атомов, параллельным переносом которой можно заполнить пространство, представляет собой прямоугольный параллелепипед с различными размерами по всем трем осям и определенным расположением атомов железа и углерода в ячейке.
В легированных сталях могут возникать соединения с химической формулой, аналогичной формуле цементита, но с частью атомов железа, замещенных атомами легирующего элемента. Такие соединения носят название специальных карбидов.
Лев Миркин
Компоненты в системе железо углерод
Аустенит
Атомы размещается в гранецентрированной ячейке. Твердость аустенита имеет твердость 200 … 250 единиц по Бринеллю. Кроме того у него хорошая пластичность и он отличается парамагнитностью.
Железо
Железо – это материал, относящийся к металлам. Его натуральный цвет – серебристо-серый. В чистом виде он очень пластичен. Его удельный вес составляет 7,86 г/куб. см. Температура плавления составляет 1539 °C. На практике чаще всего применяют техническое железо, в составе которого присутствуют следующие примеси – марганец, кремний и многие другие. Массовая доля примесей не превышает 0,1%.

Железо
У железа есть такое свойство как полиформизм. То есть, при одном и том же химическом составе, это вещество может иметь разную структуру кристаллической решетки и соответственно разные свойства. Модификации железа называют соответственно – Б, Г, Д. Все эти модификации существуют при разных условиях. Например, тип Б, может существовать только при температуре 911 °С. Тип Г может существовать в диапазоне от 911 до 1392 °С. Тип Д существует в диапазоне от 1392 до 1539 °С.
Каждый из типов обладает своей формой кристаллической решеткой, например, у типа Б решетка представляет собой куб, решетка типа Г имеет гранецентрированную кубическую форму. Решетка типа Д, имеет форму объемно центрированного куба.
Еще одно свойство состоит в том, что при температуре ниже 768 железо ферримагнитно, а при ее повышении это свойство теряется.
Точки полиморфной и магнитной трансформации называют критическими. На таблице они обозначены следующим образом – А2, А3, А4. Цифровые индексы показывают тип трансформации. Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.
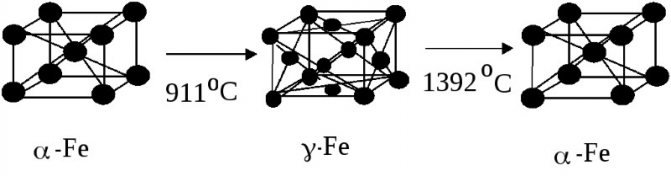
Полиморфные модификации железа
При высоких параметрах пластичности, железо не обладает высокой твердостью, по шкале Бринелля она равна 80 единиц.
Железо имеет возможность образовывать твердые растворы. Их можно разделить на две группы – раствор замещения и внедрения. Первые состоят их железа и других металлов, вторые из железа и углерода, водорода и азота.
Углерод
Другой компонент системы – углерод. Это – неметалл и он обладает тремя модификациями в виде алмаза, графита и угля. Он плавится при 3500 °С.
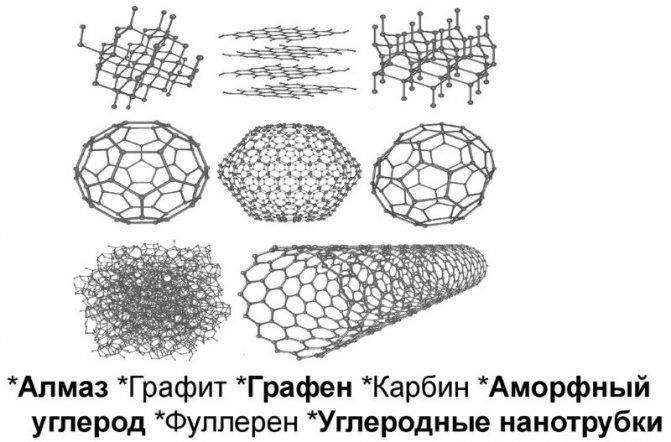
Аллотропные модификации углерода
В сплаве железа, этот элемент находится в виде твердого раствора, его называют цементит или в виде графита. В таком виде он присутствует в сером чугуне. Графит, не отличается ни пластичностью, ни прочностью.
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита
Этот процесс имеет важное практическое значение при структурообразовании чугунов
Структурные составляющие железоуглеродистых сплавов
Основными компонентами, от которых зависит структура и свойства железоуглеродистых сплавов, являются железо и углерод. Чистое железо – металл серебристо-белого цвета; температура плавления 1539°С. Железо имеет две полиморфные модификации: α и γ. Модификация α существует при температурах ниже 911°С и выше 1392°С; γ-железо – при 911-1392°С.
В зависимости от температуры и концентрации углерода железоуглеродистые сплавы имеют следующие структурные составляющие.
- Феррит (Ф) – твердый раствор внедрения углерода в α-железе. Растворимость углерода в α-железе при комнатной температуре до 0,005%; наибольшая растворимость – 0,02% при 727°С. Феррит имеет незначительную твердость (НВ 80-100) и прочность (σв=250 МПа), но высокую пластичность (δ=50%; φ=80%).
- Аустенит (А) – твердый раствор внедрения углерода в γ-железе. В железоуглеродистых сплавах он может существовать только при высоких температурах. Предельная растворимость углерода в γ-железе 2,14% при температуре 1147°С и 0,8% – при 727°С. Эта температура является нижней границей устойчивого существования аустенита в железоуглеродистых сплавах. Аустенит имеет твердость НВ 160-200 и весьма пластичен (δ=40-50%).
- Цементит (Ц) – химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67% углерода. Температура плавления цементита около 1600°С. Он очень тверд (НВ~800), хрупок и практически не обладает пластичностью. Цементит неустойчив и в определенных условиях распадается, выделяя свободный углерод в виде графита по реакции Fe3C→3Fe+C.
- Графит – это свободный углерод, мягок (НВ 3) и обладает низкой прочностью. В чугунах и графитизированной стали содержится в виде включений различных форм (пластинчатой, шаровидной и др.). С изменением формы графитовых включений меняются механические и технологические свойства сплава.
- Перлит (П) – механическая смесь (эвтектоид, т. е. подобный эвтектике, но образующийся из твердой фазы) феррита и цементита, содержащая 0,8% углерода. Перлит может быть пластинчатым и зернистым (глобулярным), что зависит от формы цементита (пластинки или зерна) и определяет механические свойства перлита. При комнатной температуре зернистый перлит имеет предел прочности σв=800 МПа; относительное удлинение δ=15%; твердость НВ 160. Перлит образуется следующим образом. Пластинка (глобуль) цементита начинает расти или от границы зерна аустенита, или центром кристаллизации является неметаллическое включение. При этом соседние области обедняются углеродом и в них образуется феррит. Этот процесс приводит к образованию зерна перлита, состоящего из параллельных пластинок или глобулей цементита и феррита. Чем грубее и крупнее выделения цементита, тем хуже механические свойства перлита.
- Ледебурит (Л) – механическая смесь (эвтектика) аустенита и цементита, содержащая 4,3% углерода. Ледебурит образуется при затвердевании жидкого расплава при 1147°С. Ледебурит имеет твердость НВ 600-700 и большую хрупкость. Поскольку при температуре 727°С аустенит превращается в перлит, то это превращение охватывает и аустенит, входящий в состав ледебурита. Вследствие этого при температуре ниже 727°С ледебурит представляет собой уже не смесь аустенита с цементом, а смесь перлита с цементитом.
Помимо перечисленных структурных составляющих в железоуглеродистых сплавах могут быть нежелательные неметаллические включения: окислы, нитриды, сульфиды, фосфиды – соединения с кислородом, азотом, серой и фосфором. На их основе могут образовываться новые структурные составляющие, например фосфидная эвтектика (Fe+Fe3P+Fe3C) с температурой плавления 950°С. Она образуется при большом содержании фосфора в чугуне. При содержании фосфора около 0,5-0,7% фосфидная эвтектика в виде сплошной сетки выделяется по границам зерен и повышает хрупкость чугуна.
СТРУКТУРА

Две модификации кристаллической решетки железа
Для железа установлено несколько полиморфных модификаций, из которых высокотемпературная модификация – γ-Fe(выше 906°) образует решетку гранецентрированного куба типа Сu (а = 3,63), а низкотемпературная – α-Fe-решетку центрированного куба типа α-Fe (a = 2,86).
В зависимости от температуры нагрева железо может находиться в трех модификациях, характеризующихся различным строением кристаллической решетки:
- В интервале температур от самых низких до 910°С —а-феррит (альфа-феррит), имеющий строение кристаллической решетки в виде центрированного куба;
- В интервале температур от 910 до 1390°С — аустенит, кристаллическая решетка которого имеет строение гранецентрированного куба;
- В интервале температур от 1390 до 1535°С (температура плавления) — д-феррит (дельта-феррит). Кристаллическая решетка д-феррита такая же, как и а-феррита. Различие между ними только в иных (для д-феррита больших) расстояниях между атомами.
При охлаждении жидкого железа первичные кристаллы (центры кристаллизации) возникают одновременно во многих точках охлаждаемого объема. При последующем охлаждении вокруг каждого центра надстраиваются новые кристаллические ячейки, пока не будет исчерпан весь запас жидкого металла.
В результате получается зернистое строение металла. Каждое зерно имеет кристаллическую решетку с определенным направлением его осей.
При последующем охлаждении твердого железа при переходах д-феррита в аустенит и аустенита в а-феррит могут возникать новые центры кристаллизации с соответствующим изменением величины зерна
Элементы диаграммы железо-углерод
Краткая информация о каждом из этих элементов.
Железо – это серебристо-серый металл. Удельный вес — 7, 86 г/см3. Имеет температуру плавления 1539° С.
При взаимодействии железа и других металлов образуются соединения, называемые растворами замещения. Если с неметаллами, например с углеродом или водородом, то — растворами внедрения.
Железо имеет способность, будучи изначально твердым, находиться в нескольких состояниях, которые в металловедении принято называть «альфа» и «гамма». Это качество называется полиморфизмом. Об этом далее в статье.
Углерод – это неметалл. Если он выступает как графит, то температура плавления равна 3500° С. Если как алмаз — 5000° С. Плотность углерода — 2,5 г/см3. Он также обладает полиморфическими свойствами.
В сплавах железо-углерод этот элемент образует твердый раствор, в составе которого есть феррум, называемый цементитом (Fe3C). Также формирует графит в чугунах.
Метастабильная диаграмма железо-цементит
Метастабильную диаграмму называют также «цементитной». Отличие от стабильной («графитной») диаграммы возникают при выделении углерода – в виде графита или цементита.
Как показано на двойной диаграмме, решетки аллотропных форм железа (δ, γ и α или дельта, гамма и альфа) служат «растворителем» для образования соответственно твердых δ-, γ- и α-растворов углерода в железе.
Когда железо с очень малым содержанием углерода кристаллизуется, то кристаллы твердого дельта-раствора выделяются по линии ликвидус АВ и линии солидус АН. Твердый дельта-раствор имеет объемноцентрированную кубическую (ОЦК) решетку – точно такую же как и твердый альфа-раствор. При максимальной температуре твердого дельта-раствора 1490 ˚С содержание углерода составляет 0,1 % (точка Н). При температуре 1490 ˚С происходит перитектическая реакция между пересыщенным твердым δ-раствором и жидкой фазой, содержащей 0,5 % углерода (точка В). В результате образуется твердый γ-раствор углерода в железе. Он содержит 0,18 % углерода (точка I).
Если содержание углерода выше, чем 0,5 %, то твердый γ-раствор кристаллизуется прямо из жидкой фазы (по линии ликвидуса ВС и линии солидуса IE). При температуре 1130 ˚С ограниченная растворимость углерода в γ-железе составляет около 2,0 % (точка Е). Снижение температуры ниже 1130 ˚С приводит к снижению растворимости углерода в γ-железе по линии ЕS. При температуре 723 ˚С растворимость углерода составляет 0,8 % (точка S). Линия ES соответствует выделению карбида железа (цементита) из γ-железа.
При повышении содержания углерода температура, при которой гамма-решетка превращается в альфа-решетку снижается и это превращение происходит в интервале температуры, соответствующем линиям GS и GP.
Линия выделения альфа-фазы GS пересекается с линией выделения карбида железа ES в точке S. Точка S является эвтектической точкой со следующими координатами: 723 ˚С по температуре и 0,80 % по содержанию углерода. В этой точке из гамма-раствора эвтектоидного состава одновременно выделяются твердый альфа-раствор (феррит) и карбид железа (цементит).
Решетка твердого альфа-раствора является идентичной решетке твердого дельта-раствора. При эвтектоидной температуре 723 ˚С твердый альфа-раствор содержит 0,02 % углерода (точка Р). Дальнейшее охлаждение приводит к понижению растворимости углерода в альфа-железе и при комнатной температуре она составляет только малые доли процента (точка D).
Когда содержание углерода составляет от 2,0 до 4,3 %, кристаллизация начинается с выделения гамма-раствора по линии ВС. Увеличение содержания углерода выше 4,3% приводит к выделению карбида железа по линии CD.
Выделение дополнительной первичной фазы в сплавах с содержанием углерода выше 2,0 % сопровождается эвтектической кристаллизацией гамма-раствора и карбида углерода в точке С, координаты которой – 1130 °С и 4,3 % углерода.
Линия МО связана с магнитным превращением, то есть переходом от ферромагнитного к парамагнитному состоянию железа.
Отжиг стали
Практикуется использование нескольких методов отжига. Принципиально различаются техники полного и неполного отжига. В первом случае происходит интенсивный нагрев аустенита до критической температуры, после чего осуществляется нормализация посредством охлаждения. Тут же происходит распад аустенита. Как правило, полный отжиг сталей производится в режиме 700-800 °С. Термическая обработка на таком уровне как раз активизирует процессы распада элементов феррита. Скорость охлаждения тоже поддается регулировке, например, обслуживающий печь персонал может управлять дверцей камеры, закрывая или открывая ее. Новейшие модели изотермических печей в автоматическом режиме могут осуществлять замедленное охлаждение в соответствии с заданной программой.

Что касается неполного отжига, то он производится при нагреве с температурой выше 800 °С. Однако имеют место серьезные ограничения по времени удержания критического температурного воздействия. По этой причине происходит неполный отжиг, в результате которого феррит не исчезает. Следовательно, не устраняется и множество недостатков структуры будущего материала. Зачем же нужен такой отжиг сталей, если он не улучшает физические качества? На самом деле именно неполная термическая обработка позволяет сохранить мягкую структуру. Конечный материал, возможно, потребуется не в каждой сфере применения, характерной для углеродистых сталей как таковых, но зато позволит с легкостью произвести механическую обработку. Мягкий доэвтектоидный сплав без особых затруднений поддается резке и дешевле обходится в процессе изготовления.
Компоненты в системе «железо-углерод»
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит:
Железо
Железо – d-переходный металл серебристо-светлого цвета. Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3. Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри. Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв=250 МПа, предел текучести – σт=120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ=50 %, а относительное сужение – ψ=80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита
Этот процесс имеет важное практическое значение при структурообразовании чугунов
Фазы в системе “железо-углерод”
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 80 – 130 НВ, временное сопротивление – σв=300 МПа) и пластичен (относительное удлинение – δ=50 %), магнитен до 768° С.
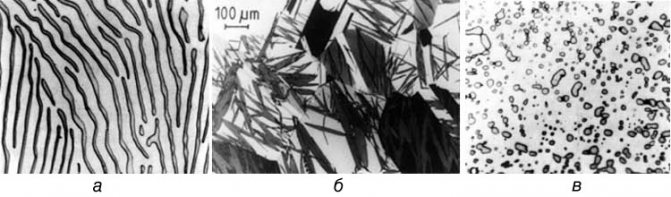
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Аустенит (А, γ) – твердый раствор внедрения углерода в γ–железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо – цементит и железо – графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе – С) – графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура – содержание углерода. Диаграмма состояния системы железо – углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран. Особое место среди них занимают работы Д.К. Чернова
Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
Диаграмма состояния железо-углерод
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус – по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % – к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии GS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) – как Аr1.
Выводы
Достичь абсолютного равновесия, как физического, так и химического, невозможно, кроме как в специальных лабораторных условиях.
На практике равновесие может быть приближено к абсолютному, но при определенных условиях: достаточно медленного повышения или понижения температуры сплава, который будет длительно выдерживаться по времени.
Источники
- https://FB.ru/article/340918/diagramma-jeleza-ugleroda-diagramma-sostoyaniya-sistemyi-jelezo-uglerod
- https://PokVorota3.ru/prokat/zhelezo-uglerod-2.html
- https://intehstroy-spb.ru/spravochnik/diagramma-sostoyaniya-zhelezo-uglerod-2.html
- https://NiceSpb.ru/materialy/diagramma-zhelezo.html
- https://pressadv.ru/stali/zhelezo-uglerod.html
- https://wiki2.org/ru/%D0%94%D0%B8%D0%B0%D0%B3%D1%80%D0%B0%D0%BC%D0%BC%D0%B0_%D1%81%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%B8%D1%8F_%D1%81%D0%BF%D0%BB%D0%B0%D0%B2%D0%BE%D0%B2_%D0%B6%D0%B5%D0%BB%D0%B5%D0%B7%D0%BE-%D1%83%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4
- https://generator98.ru/raboty-so-stalyu/tablica-zhelezo-uglerod.html


























