Кипение и плавление металла
Переход ртути в жидкое состояние происходит в специальных термометрах
Технология физико-химических исследований при условиях высоких температур рассматривает давление плавления металла при разных температурах. Точность опытов обеспечивает применение на практике свойств химического элемента № 80.
Для измерения температуры выше +360°C пользуются термопарами или специальными термометрами, в которых пространство надо ртутью заполнено газом. С целью повышения температуры кипения металла в капилляр надо ртутью закачивают азот. При давлении 30 атмосфер температурный градиент увеличивается до +600°C.
Такого типа термометры требуют постепенного нагрева. Нижним пределом такого измерительного прибора является температура перехода живого серебра в твердое состояние.
Теплоемкость металла с увеличением температуры последовательно уменьшается и после определенного порога температурного градиента начинает медленно расти. Это свойство и жидкое состояние роднит ртуть с водой.
Таблица характеристик
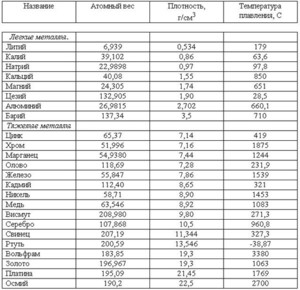 Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C. Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия — 2519 °C, у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов — у рения — 5596 °C. Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов. Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Сплавы металлов
Чтобы проектировать изделия из сплавов, сначала изучают их свойства. Для изучения в небольших емкостях расплавляют изучаемые металлы в разном соотношении между собой. По итогам строят графики.
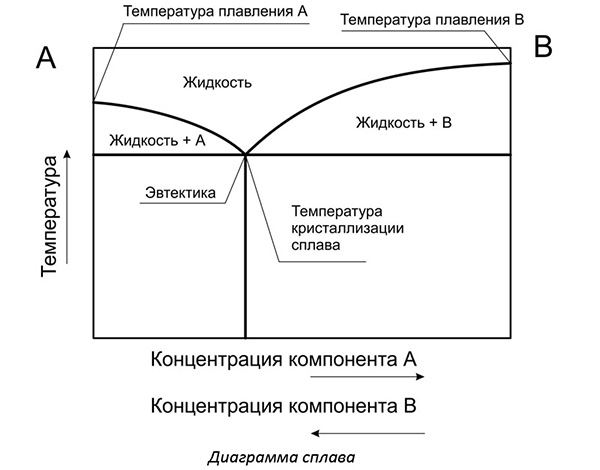
Нижняя ось представляет концентрацию компонента А с компонентом В. По вертикали рассматривают температуру. Здесь отмечают значения максимальной температуры, когда весь металл находится в расплавленном состоянии.
При охлаждении один из компонентов начинает образовывать кристаллы. В жидком состоянии находится эвтектика – идеальное соединение металлов в сплаве.
Металловеды выделяют особое соотношение компонентов, при котором температура плавления минимальная. Когда составляют сплавы, то стараются подбирать количество используемых веществ, чтобы получать именно эвтектоидный сплав. Его механические свойства наилучшие из возможных. Кристаллические решетки образуют идеальные гранецентрированные положения атомов.
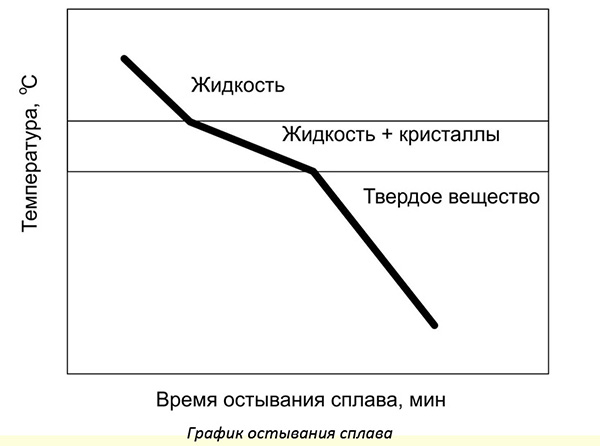
Изучают процесс кристаллизации путем исследования твердения образцов при охлаждении. Строят специальные графики, где наблюдают, как изменяется скорость охлаждения. Для разных сплавов имеются готовые диаграммы. Отмечая точки начала и конца кристаллизации, определяют состав сплава.
Тугоплавкие металлы
Температура тугоплавких металлов выше 1600°C. Это вольфрам, титан, платина, хром и другие. Их используют в качестве источников света, машинных деталей, смазочных материалов, а также в ядерной промышленности. Из них изготавливают проволоки, высоковольтные провода и используют для расплавки других металлов с более низкой температурой плавления. Платина начинает переходить из твердого в жидкое состояние при температуре 1769 градусов, а вольфрам – при температуре 3420°C.
Ртуть – единственный металл, находящийся в жидком состоянии при обычных условиях, а именно, нормальном атмосферном давлении и средней температуре окружающей среды. Температура плавления ртути составляет минус 39°C. Этот металл и его пары являются ядовитыми, поэтому он используется только в закрытых емкостях или в лабораториях. Распространенное применение ртути – градусник для измерения температуры тела.
Каждый металл и сплав имеет собственный уникальный набор физических и химических свойств, среди которых не последнее место занимает температура плавления. Сам процесс означает переход тела из одного агрегатного состояния в другое, в данном случае, из твердого кристаллического состояния в жидкое. Чтобы расплавить металл, необходимо подводить к нему тепло до достижения температуры плавления. При ней он все еще может оставаться в твердом состоянии, но при дальнейшем воздействии и повышении тепла металл начинает плавиться. Если температуру понизить, то есть отвести часть тепла, элемент затвердеет.
Самая высокая температура плавления среди металлов принадлежит вольфраму: она составляет 3422С о , самая низкая — у ртути: элемент плавится уже при — 39С о . Определить точное значение для сплавов, как правило, не представляет возможности: оно может значительно колебаться в зависимости от процентного соотношения компонентов. Их обычно записывают в виде числового промежутка.
Ртуть (-38,87°C)

Все мы хорошо знакомы со ртутью — даже сегодня, в век электроники, вряд ли найдётся хоть один человек, которому не измеряли бы температуру тела ртутным термометром. Но мало кто задумывается, что очень текучая тяжёлая серебристая жидкость — самый настоящий металл!
Да-да, элемент №80, Hydrargyrum, плавится на самом лютом морозе — температура кристаллизации ртути почти минус сорок градусов (-38,87°C).
Человечество знакомо со ртутью с древнейших времён. Ртуть находит широчайшее применение в технике, химии, металлургии. Этот элемент достоин отдельного, немаленького рассказа — а сегодня он гордо венчает наш рейтинг.
Температуры плавления и кипения чистых химических элементов при атмосферном давлении
Обозначения: (Т.Р. тройная точка).
Литература: Bulletin of Alloy Phase Diagrams.
| Символ элемента | Температура,
плавления, °C |
Температура
плавления, K |
погрешность | Температура
кипения, °C |
Температура
кипения, K |
| Ac | 1051 | 1324 | ±50 | 3200 | 3473(a) |
| Ag | 961.93 | 1235.08 | — | 2163 | 2436 |
| Al | 660.452 | 933.602 | — | 2520 | 2793 |
| Am | 1176 | 1449 | — | — | — |
| Ar | -189.352(T.P.) | 83.798(T.P.) | — | -185.9 | 87.3 |
| As | 614(S.P.) | 887(S.P.) | — | — | — |
| At | -302 | -575 | — | — | — |
| Au | 1064.43 | 1337.58 | — | 2857 | 3130 |
| B | 2092 | 2365 | — | 4002 | 4275 |
| Ba | 727 | 1000 | ±2 | 1898 | 2171 |
| Be | 1289 | 1562 | ±5 | 2472 | 2745 |
| Bi | 271.442 | 544.592 | — | 1564 | 1837 |
| Bk | 1050 | 1323 | — | — | — |
| Br | -7.25(T.P.) | 265.90(T.P.) | — | 59.10 | 332.25 |
| C | 3827(S.P.) | 4100(S.P.) | ±50 | — | — |
| Ca | 842 | 1115 | ±2 | 1484 | 1757 |
| Cd | 321.108 | 594.258 | — | 767 | 1040 |
| Ce | 798 | 1071 | ±3 | 3426 | 3699 |
| Cf | 900 | 1173 | — | — | — |
| Cl | -100.97(T.P.) | 172.18(T.P.) | — | -34.05 | 239.10 |
| Cm | 1345 | 1618 | — | — | — |
| Co | 1495 | 1768 | — | 2928 | 3201 |
| Cr | 1863 | 2136 | ±20 | 2672 | 2945 |
| Cs | 28.39 | 301.54 | ±0.05 | 671 | 944 |
| Cu | 1084.87 | 1358.02 | ±0.04 | 2563 | 2836 |
| Dy | 1412 | 1685 | — | 2562 | 2835 |
| Er | 1529 | 1802 | — | 2863 | 3136 |
| Es | 860 | 1133 | — | — | — |
| Eu | 822 | 1095 | — | 1597 | 1870 |
| F | -219.67(T.P.) | 53.48(T.P.) | — | -188.20 | 84.95 |
| Fe | 1538 | 1811 | — | 2862 | 3135 |
| Fm | -1527 | -1800 | — | — | — |
| Fr | -27 | -300 | — | — | — |
| Ga | 29.7741(T.P.) | 302.9241(T.P.) | ±0.001 | 2205 | 2478 |
| Gd | 1313 | 1586 | — | 3266 | 3539 |
| Ge | 938.3 | 1211.5 | — | 2834 | 3107 |
| H | -259.34(T.P.) | 13.81(T.P.) | — | -252.882 | 20.268 |
| He | -271.69(T.P.) | 1.46(T.P.) | (b) | -268.935 | 4.215 |
| Hf | 2231 | 2504 | ±20 | 4603 | 4876 |
| Hg | -38.8290 | 234.314 | — | 356.623 | 630 |
| Ho | 1474 | 1747 | — | 2695 | 2968 |
| I | 113.6 | 386.8 | — | 185.25 | 458.40 |
| In | 156.634 | 429.784 | — | 2073 | 2346 |
| Ir | 2447 | 2720 | — | 4428 | 4701 |
| K | 63.71 | 336.86 | ±0.5 | 759 | 1032 |
| Kr | -157.385 | 115.765 | ±0.001 | -153.35 | 119.80 |
| La | 918 | 1191 | — | 3457 | 3730 |
| Li | 180.6 | 453.8 | ±0.5 | 1342 | 1615 |
| Lr | -1627 | -1900 | — | — | — |
| Lu | 1663 | 1936 | — | 3395 | 3668 |
| Md | -827 | -1100 | — | — | — |
| Mg | 650 | 923 | ±0.5 | 1090 | 1363 |
| Mn | 1246 | 1519 | ±5 | 2062 | 2335 |
| Mo | 2623 | 2896 | — | 4639 | 4912 |
| N | -210.0042(T.P.) | 63.1458(T.P.) | ±0.0002 | -195.80 | 77.35 |
| Na | 97.8 | 371.0 | ±0.1 | 883 | 1156 |
| Nb | 2469 | 2742 | — | 4744 | 5017 |
| Nd | 1021 | 1294 | — | 3068 | 3341 |
| Ne | -248.587(T.P.) | 24.563(T.P.) | ±0.002 | -246.054 | 27.096 |
| Ni | 1455 | 1728 | — | 2914 | 3187 |
| No | -827 | -1100 | — | — | — |
| Np | 639 | 912 | ±2 | — | — |
| O | -218.789(T.P.) | 54.361(T.P.) | — | -182.97 | 90.18 |
| Os | 3033 | 3306 | ±20 | 5012 | 5285 |
| P(white) | 44.14 | 317.29 | ±0.1 | 277 | 550 |
| P(red) | 589.6(T.P.) | 862.8(T.P.) | (c) | 431 | 704 |
| Pa | 1572 | 1845 | — | — | — |
| Pb | 327.502 | 600.652 | — | 1750 | 2023 |
| Pd | 1555 | 1828 | ±0.4 | 2964 | 3237 |
| Pm | 1042 | 1315 | — | — | — |
| Po | 254 | 527 | — | — | — |
| Pr | 931 | 1204 | — | 3512 | 3785 |
| Pt | 1769.0 | 2042.2 | — | 3827 | 4100 |
| Pu | 640 | 913 | ±1 | 3230 | 3503 |
| Ra | 700 | 973 | — | — | — |
| Rb | 39.48 | 312.63 | ±0.5 | 688 | 961 |
| Re | 3186 | 3459 | ±20 | 5596 | 5869 |
| Rh | 1963 | 2236 | — | 3697 | 3970 |
| Rn | -71 | 202 | — | -62 | 211 |
| Ru | 2334 | 2607 | ±10 | 4150 | 4423 |
| S | 115.22 | 388.37 | — | 444.60 | 717.75 |
| Sb | 630.755 | 903.905 | — | 1587 | 1860 |
| Sc | 1541 | 1814 | — | 2831 | 3104 |
| Se | 221 | 494 | — | 685 | 958 |
| Si | 1414 | 1687 | ±2 | 3267 | 3540 |
| Sm | 1074 | 1347 | — | 1791 | 2064 |
| Sn | 231.9681 | 505.1181 | — | 2603 | 2876 |
| Sr | 769 | 1042 | — | 1382 | 1655 |
| Ta | 3020 | 3293 | — | 5458 | 5731 |
| Tb | 1356 | 1629 | — | 3223 | 3496 |
| Tc | 2155 | 2428 | ±50 | 4265 | 4538 |
| Te | 449.57 | 722.72 | ±0.3 | 988 | 1261 |
| Th | 1755 | 2028 | ±10 | 4788 | 5061 |
| Ti | 1670 | 1943 | ±6 | 3289 | 3562 |
| Tl | 304 | 577 | ±2 | 1473 | 1746 |
| Tm | 1545 | 1818 | — | 1947 | 2220 |
| U | 1135 | 1408 | — | 4134 | 4407 |
| V | 1910 | 2183 | ±6 | 3409 | 3682 |
| W | 3422 | 3695 | — | 5555 | 5828 |
| Xe | -111.7582(T.P.) | 161.3918(T.P.) | ±0.0002 | -108.12 | 165.03 |
| Y | 1522 | 1795 | — | 3338 | 3611 |
| Yb | 819 | 1092 | — | 1194 | 1467 |
| Zn | 419.58 | 692.73 | — | 907 | 1180 |
| Zr | 1855 | 2128 | ±5 | 4409 | 4682 |
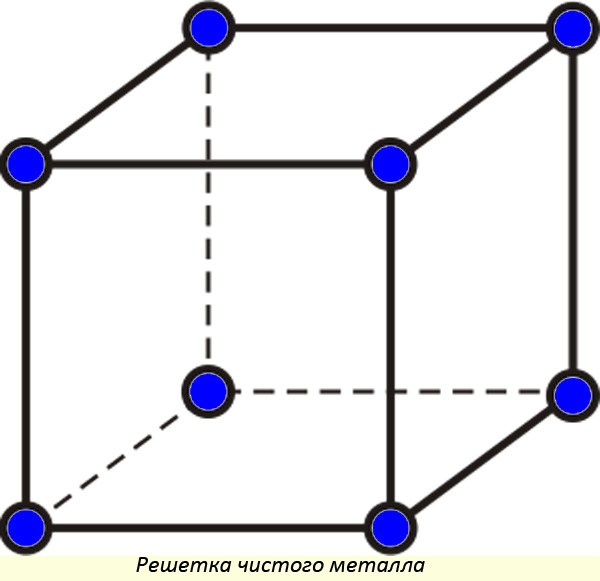
Кристаллические решетки металла
В идеальном виде принято считать, что металлам свойственна кубическая решетка (в реальном веществе могут быть изъяны). Между молекулами имеются равные расстояния по горизонтали и вертикали.
Твердое вещество характеризуется постоянством:
- формы, предмет сохраняет линейные размеры в разных условиях;
- объема, предмет не изменяет занимаемое количество вещества;
- массы, количество вещества, выраженное в граммах (килограммах, тоннах);
- плотности, в единице объема содержится постоянная масса.
При переходе в жидкое состояние, достигнув определенной температуры, кристаллические решетки разрушаются. Теперь нельзя говорить о постоянстве формы. Жидкость будет принимать ту форму, в какую ее зальют.
Когда происходит испарение, то постоянным остается только масса вещества. Газ займет весь объем, который будет ему предоставлен. Здесь нельзя утверждать, что плотность постоянная величина.
Когда соединяются жидкости, то возможны варианты:
- Жидкости полностью растворяются одна в другой, так себя ведут вода и спирт. Во всем объеме концентрация веществ будет одинаковой.
- Жидкости расслаиваются по плотности, соединение происходит только на границе раздела. Только временно можно получать механическую смесь. Перемешав разные по свойствам жидкости. Примером является масло и вода.
Металлы образуют сплавы в жидком состоянии. Чтобы получить сплав, каждый из компонентов должен быть в жидком состоянии. У сплавов возможны явления полного растворения одного в другом. Не исключаются варианты, когда сплав будет получен только в результате интенсивного перемешивания. Качество сплава в этом случае не гарантируется, поэтому стараются не смешивать компоненты, которые не позволяют получать стабильные сплавы.
Образующиеся растворимые друг в друге вещества при застывании образуют кристаллические решетки нового типа. Определяют:
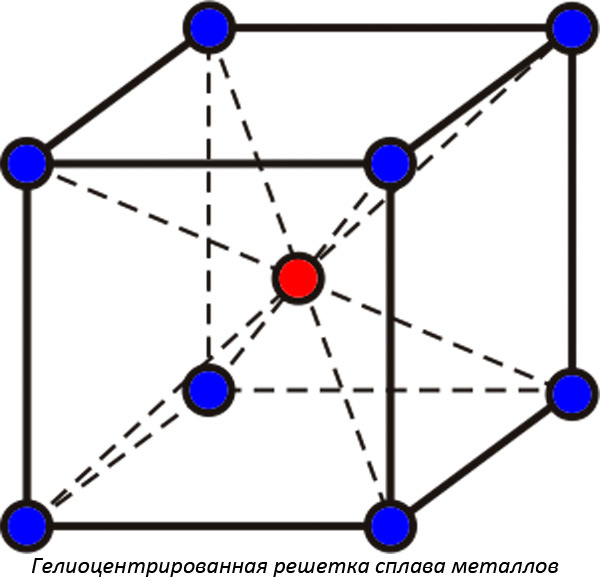
- Гелиоцентрированные кристаллические решетки, их еще называют объёмно-центрированными. В середине находится молекула одного вещества, а вокруг располагаются еще четыре молекулы другого. Принято называть подобные решетки рыхлыми, так как в них связь между молекулами металлов слабее.
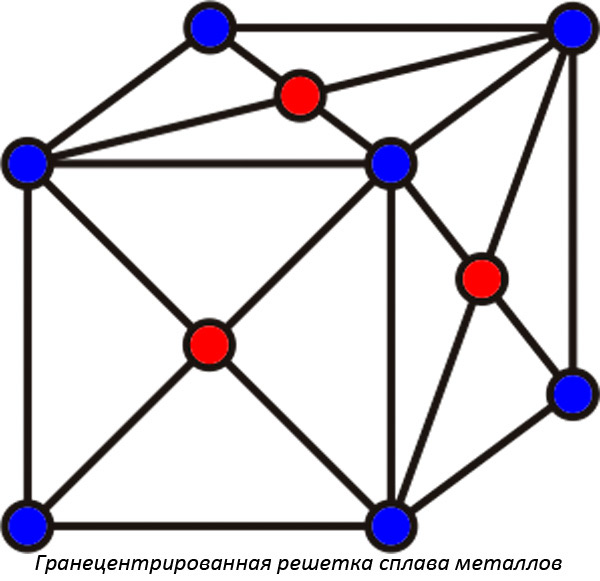
- Гранецентрированные кристаллические решетки образуют соединения, в которых молекулы компонента располагаются на гранях. Металловеды называют подобные кристаллические сплавы плотными. В реальности плотность сплава может быть выше, чем у каждого из входящих в состав компонентов (алхимики средних веков искали варианты сплавов, при которых плотность будет соответствовать плотности золота).
Сплавы металлов
Чтобы проектировать изделия из сплавов, сначала изучают их свойства. Для изучения в небольших емкостях расплавляют изучаемые металлы в разном соотношении между собой. По итогам строят графики.
Нижняя ось представляет концентрацию компонента А с компонентом В. По вертикали рассматривают температуру. Здесь отмечают значения максимальной температуры, когда весь металл находится в расплавленном состоянии.
При охлаждении один из компонентов начинает образовывать кристаллы. В жидком состоянии находится эвтектика – идеальное соединение металлов в сплаве.
Металловеды выделяют особое соотношение компонентов, при котором температура плавления минимальная. Когда составляют сплавы, то стараются подбирать количество используемых веществ, чтобы получать именно эвтектоидный сплав. Его механические свойства наилучшие из возможных. Кристаллические решетки образуют идеальные гранецентрированные положения атомов.
Изучают процесс кристаллизации путем исследования твердения образцов при охлаждении. Строят специальные графики, где наблюдают, как изменяется скорость охлаждения. Для разных сплавов имеются готовые диаграммы. Отмечая точки начала и конца кристаллизации, определяют состав сплава.
Способы прокаливания алюминиевой сковороды
Способы придуманы и применяются людьми очень давно, когда еще не было антипригарных покрытий. Цель процедуры по подготовке к первому использованию – закупоривание пор и создание своеобразной защитной пленки. Дело в том, что алюминий имеет микропоры, поэтому и возникает пригорание. Прокаливание помогает их заполнить до появления момента прилипания готовящихся блюд ко дну.
«Бабушкин» метод с помощью соли
Наиболее распространенный и простой вариант подготовки к первому использованию:
- Чистую, насухо вытертую сковороду поставьте на плиту и сделайте максимально слабый огонь.
- Дно засыпьте крупной поваренной солью слоем приблизительно 1 см.
- Подогревайте 20 минут, затем дайте полностью остыть.
- Освободите дно от соли и протрите мягкой тряпочкой, пропитанной рафинированным растительным маслом.
- Пользуйтесь через 2-3 дня.
Вариант с водой без соли
Прокипятите воду в сковороде, затем слейте. Оставьте высыхать естественным путем, не вытирая. Нанесите равномерно на поверхность растительное масло и не пользуйтесь обработанной алюминиевой посудой несколько дней.
Прокаливание растительным маслом
Не менее распространенный метод подготовки новой алюминиевой сковороды к использованию заключается в следующем:
- Налейте растительное масло в таком количестве, чтобы дно было полностью покрыто.
- На медленном огне подогревайте его в среднем 20-25 минут.
- После остывания ополосните чистой водой без применения химических средств.
- Пользуйтесь посудой спустя время (1-2 дня).
Перед работой установите вытяжку на максимальный режим, откройте окна, так как во время разогревания появится характерный запах. Обязательно используйте рафинированное масло, иначе будет очень много дыма.
Комбинированный метод
Этот способ совмещает два предыдущих, в которых используется масло и соль. Хороший эффект получается, если взять два ингредиента одновременно. Для этого на этапе начала подогревания масла добавьте в него столовую ложку соли. Спустя 20 минут прекратите нагрев, дайте остыть, ополосните.
Цинк
Упрощенный способ
Самый экономный по времени вариант подготовки алюминиевой сковородки к первой готовке, так как не нужно стоять около плиты. Суть заключается в прокаливании в духовке:
- Чистую сковородку предварительно смажьте с обеих сторон рафинированным маслом.
- Поместите ее вверх дном в предварительно нагретую на 180 градусов духовку.
- Спустя один час выключите духовку и оставьте там сковороду остывать.
- Через несколько дней начинайте пользоваться новой антипригарной посудой.
Температура плавления стали
Видео: Как делают нержавеющую сталь ?
Прежде чем говорить о сталях, давайте определимся с физическим смыслом самой категории температура плавления. В научно-производственной сфере это понятие используется еще и как температура отвердевания. Физический смысл данной категории состоит в том, что эта температура показывает, при каком ее значении происходит смена агрегатного состояния вещества, то есть его переход из жидкого в твердое состояние. В самой же точке температурного перехода вещество может быть как в одном, так и в другом состоянии. При подаче дополнительного тепла предмет или вещество приобретает жидкое состояние, а при отведении тепла – отвердевает
Этот показатель считается одним из самых важных в системе физических свойств любого вещества, при этом необходимо учитывать (это особенно важно понимать применительно к сталям), что температура отвердевания численно равна температуре плавления лишь в том случае, когда мы говорим об идеально чистом веществе
Видео: С.С. Плавка стали, очень дёшево и просто!!!
Как известно из школьной программы, температура плавления стали для различных видов сплавов различна. Это определяется структурой сплава, входящими в него компонентами, характером технологического производства стали и другими факторами.
Так, например, температура плавления стали, состоящей из медноникелевого сплава равна примерно 1150 °С. Если мы будем в таком сплаве увеличивать содержание никеля, то температура будет повышаться, так как температура плавления самого никеля гораздо выше, чем у меди. Как правило, в зависимости от химического состава сплава и соотношения присутствующих в нем компонентов температура плавления стали может находиться в границах 1420-1525 °С, если такая сталь подлежит разливке в формы в процессе металлургического производства, то температуру необходимо поддерживать еще на 100-150 градусов выше. Важным фактором, который влияет на температуру плавления, является уровень содержания в сплаве углерода. Если его содержание высоко, то температура будет ниже, и, соответственно, наоборот – при понижении количества углерода температура повышается.
Видео: Температура металла по цвету свечения. Хороший способ.
Более сложным с точки зрения определения величины является процесс измерения температуры плавления в нержавеющих сталях. Причиной этого является их сложный химический состав. Например, стали марки 1X18H9, широко используемые в стоматологии и электротехнике, имеют в своем составе, кроме собственно железа, еще углерод, никель, хром, марганец, титан и кремний. Естественно, температура плавления нержавеющей стали такого состава будет определяться свойствами каждого компонента, входящего в нее. Из такой стали изготавливаются литые зубы, коронки, различного типа зубные протезы, электродетали и другое. Можно привести перечень некоторых свойств, которыми обладает эта нержавеющая сталь, температура плавления ее составляет 1460-1500 °С, поэтому, исходя из данного параметра и химического состава сплава, для его пайки применяются специальные серебряные припои.
Одними из самых высокотехнологичных в современном производстве видов сплавов являются различные стали с включением в их состав элементов титана. Это обусловлено тем, что эти стали имеют практически стопроцентную биологическую инертность, а температура плавления стали на основе титана – одна их самых высоких.
Видео: Температура Плавления Бутылочного Стекла
Большинство сталей содержит в своем составе железо в качестве основного компонента. Это объясняется не только тем, что этот металл – один из распространенных в природной среде, а еще и тем, что железо представляет собой практически универсальный элемент для производства сталей различных марок и сплавов, в состав которых он входит. Эта широта применения объясняется тем, что показатель температуры плавления этого металла, равный 1539 градусам, в сочетании с иными уникальными химическими свойствами делает железо подходящим компонентом для широкого перечня марок сталей различного назначения.
сроден
Технология производства
Поскольку «чистый» вольфрам встретить в природе нельзя (он является составной частью горных пород), то необходима процедура по выделению данного металла. Причем ученые оценивают содержание его в коре Земли так – на 1000 кг породы всего 1,3 грамма вольфрама. Можно отметить, что самый тугоплавкий металл, является довольно редким элементом, если сравнить его с известными видами металлов.
Когда из недр Земли добывается руда, то количество вольфрама в ней составляет только лишь до двух процентов. По этой причине добываемое сырье идет на обогатительные заводы, где специальными способами массовую долю металла приводят к шестидесяти процентам. При получении «чистого» вольфрама процесс делится на несколько технологических этапов. Первый заключается в выделении чистого триоксида из добытого сырья. Для данной цели используется термическое разложение, когда самая высокая температура плавления металла составляет от 500 до 800 градусов. При данном температурном режиме лишние элементы поддаются плавлению, а из расплавленной массы собирается оксид вольфрама.

Далее получившееся соединение проходит этап тщательного измельчения, а затем осуществляется восстановительная реакция. Для этого добавляется водород и используется температура в 700 градусов. В результате получается чистый металл, который имеет порошкообразный вид. Затем идет процесс спрессовывания порошка, для чего применяют высокое давление, и спекания в среде из водорода, где температурный режим составляет 1200-1300 градусов.

Получившуюся массу отправляют в специальную печь для плавления, где масса нагревается электрическим током до отметки более 3000 градусов. То есть вольфрам получается жидким после плавления. Затем масса очищается от примесей и создается монокристаллическая ее решетка. Для этого используют способ зонной плавки – его суть состоит в том, что расплавленной на некотором промежутке времени является лишь часть металла. Этот метод позволяет осуществлять процесс перераспределения примесей, который скапливаются на одном участке, откуда их легко убрать из общей структуры сплава. Необходимый вольфрам имеет вид слитков, которые и применяются для производства необходимых видов продукции в разных отраслях деятельности.
Ртуть (-38,87°C)

Все мы хорошо знакомы со ртутью — даже сегодня, в век электроники, вряд ли найдётся хоть один человек, которому не измеряли бы температуру тела ртутным термометром. Но мало кто задумывается, что очень текучая тяжёлая серебристая жидкость — самый настоящий металл!
Да-да, элемент №80, Hydrargyrum, плавится на самом лютом морозе — температура кристаллизации ртути почти минус сорок градусов (-38,87°C).
Человечество знакомо со ртутью с древнейших времён. Ртуть находит широчайшее применение в технике, химии, металлургии. Этот элемент достоин отдельного, немаленького рассказа — а сегодня он гордо венчает наш рейтинг.
1 0
От чего зависит температура плавления металла в градусах?
снижению твердости
Твердое и жидкое состояние металла
Многие знакомы с металлами и сплавами по их твердому состоянию. Они встречаются практически во всех сферах деятельности. Только в металлургии и в производственных цехах металл встречается в жидком состоянии. Это связано с тем, что для преобразования кристаллической решетки приходится проводить нагрев сырья до рекордных температур.
Твердое состояние характеризуется следующими качествами:
- Структура держит свою форму. Сталь известна тем, что может выдерживать серьезную нагрузку в течение длительного периода.
- Каждому материалу свойственны свои показатели прочности и твердости, вязкости.
- Постоянный химический состав. Поверхность стали или других сплавов может реагировать на воздействие химических веществ, окисляться или покрываться коррозий, но вот химический состав остается неизменным.
- Возможность обработки резанием. При повышении пластичности не образуется стружка на момент механической обработки, что существенно усложняет процесс.
В жидком или вязком состоянии металл приобретает совсем другие свойства:
- Высокая пластичность позволяет выполнять литье по форме, ковку или проводить другую обработку, связанную с пластической деформацией заготовок.
- Есть возможность изменить химический состав путем добавления легирующих элементов. За счет подвижной кристаллической решетки можно проводить насыщение структуры стали хромом, никелем, титаном и многими другими веществами.
- Термическая обработка проводится также при температуре, которая приводит к перестроению кристаллической решетки. Однако при закалке металл сохраняет свою форму, то есть структура остается твердой.
Существуют сплавы, которые можно разогреть до жидкого состояния и в домашних условиях. Примером можно назвать олово, применяемое при изготовлении припоя. Температура плавления олова находится в пределах 250 градусов Цельсия. Этот показатель нагрева можно достигнуть при применении обычного паяльника.
От чего может зависеть температура плавления
Для различных материалов температура, при которой происходит полное перестроение структуры до текучего состояния, разная. Если рассматривать сталь и различные сплавы, то отметим следующие зависимости:
В чистом виде металлы встречаются довольно редко. Во многом показатель температуры кипения зависит от химического состава. Примером назовем олово, в которое могут добавлять цинки, серебро и другие элементы. Примеси могут делать материал более или менее устойчивым к нагреву.
Существуют сплавы, которые из-за своего химического состава могут переходить в жидкое состояние при температуре выше 150 градусов Цельсия. Кроме этого, встречаются сплавы, структура которых может выдерживать нагрев до 3 000 градусов Цельсия и более
С учетом того, что при перестроении кристаллической решетки изменяются все физико-механические качества, а условия эксплуатации могут характеризоваться температурой нагрева, можно сказать: точка плавления металла — важное физическое свойство вещества. Примером можно назвать изготовление деталей для авиационного оборудования.
Термическая обработка, как правило, практически не изменяет устойчивость структуры к нагреву. Единственным способом повышения устойчивости к нагреву можно назвать изменение химического состава, для чего и проводится легирование стали.
https://youtube.com/watch?v=cIlonSuReH0
Важность рассматриваемого показателя
Температура плавления материалов учитывается практически во всех сферах их применения. Примером можно назвать то, что на момент рождения авиации не могли использовать обычный алюминий, так как он быстро нагревался из-за трения и терял свои линейные размеры. Появление дюралюминия существенно изменило мир авиации. После его открытия все дирижабли и самолеты стали изготавливать при обширном применении этого сплава.
ответственные детали
Существует довольно большое количество справочников, в которых указывается температура плавления для всех металлов и иных сплавов. При рассмотрении этого показателя следует учитывать химический состав. Даже незначительное изменение концентрации одного из элементов приведет к повышению или понижению температуры перестроения кристаллической решетки.






























