Реакции с элементами
Важной целью цинковых взаимодействий с неметаллами является получение бинарных неорганических соединений. Нагретая смесь цинка и серы дает в результате сульфид (ZnS). Это соединение внешне выглядит как бесцветные кристаллы
Сульфид применяют в лазерной промышленности в качестве полупроводникового материала. Прохождение паров фосфора через цинковые пластины образует ядовитое для живых организмов вещество — фосфид цинка Zn3P2. Фосфид хорошо вступает в реакцию с кислотами. В связи с этим его применяют в борьбе против хозяйственных вредителей, отравляя кислотную среду в желудке грызунов
Это соединение внешне выглядит как бесцветные кристаллы. Сульфид применяют в лазерной промышленности в качестве полупроводникового материала. Прохождение паров фосфора через цинковые пластины образует ядовитое для живых организмов вещество — фосфид цинка Zn3P2. Фосфид хорошо вступает в реакцию с кислотами. В связи с этим его применяют в борьбе против хозяйственных вредителей, отравляя кислотную среду в желудке грызунов.
При нагревании вплоть до 600 °С реакцию цинка в токе аммиака производит нитрид Zn3N2. Данное соединение является тугоплавким и часто используется в огнеупорных материалах на воздухе. Однако крайне неустойчиво к воде, которая его быстро разлагает. Существует ряд элементов, в реакцию с которыми цинк вступает только в присутствии паров воды: бром, фтор, хлор. Не взаимодействует в принципе с водородом, азотом, углеродом, кремнием и бором.
Взаимодействие с кислотами
Хорошая реакция цинка с большинством кислот обусловлена его положением по отношению к водороду в электрохимическом ряду активности металлов. Так образуется множество важных цинковых солей. Эти соли преимущественно бесцветные, представляют гигроскопичные кристаллы, растворы которых вследствие гидролиза имеют кислотную среду. В случае с солями других металлов он будет также вытеснять их из раствора, если они стоят в ряду напряжения правее от элемента.

При взаимодействии с кислотами образуются соли цинка.
В растворе элемента с серной кислотой при температуре ниже 38 °C образуется цинковый купорос, научное название которого сульфат ZnSO4. Его используют в производстве вискозы, некоторых отраслях металлургии, в медицине как обеззараживающее средство. Хлорид ZnCl2 получают из раствора соляной кислоты с цинком. Его используют в производстве батареек, антисептической пропитке дерева и бумажной фибры.
Производные соединения
- Цинк и его амфотерные свойства передаются гидроксидам цинка Zn (OH)2. Этим веществам присуще химическое поведение кислот и оснований одновременно. Получить гидроксид в виде белого осадка можно действием щелочи на сульфат. В естественном состоянии гидроксид — это кристалловидное вещество, разлагающееся при температуре свыше 130 °C. Применяется для синтеза солей цинка.
- Эффектным можно назвать старый способ добычи оксида ZnO, именуемый ранее как «французский процесс». В присутствии сильно нагретого воздуха вокруг пластины элемента начнут выделяться пары цинка, которые затем воспламеняются голубоватым светом, образуя оксид. На крупном производстве его добывают из природного минерала цинкита. Кроме того, для производства оксида широко применяют термическое разложение более сложных соединений, как, например, гидроксида.
- Бесцветный белый порошок оксида, не растворяющийся в воде, выражает свою химическую двойственность. При сплавлении оксида цинка со щелочами получают цинкаты. При сплавлении с оксидами — силикаты. Собственная теплопроводность позволяет ему быть полупроводником, ширина запрещенной зоны которого равна 3,36 эВ. Оксид имеет широкий спектр применения в химической промышленности, став наполнителем многих пластмасс. В электронике без него не обходится ни одна лучевая трубка телевизора. Он также входит в состав большинства дерматологических мазей.
Смеси и сплавы
Для усиления прочности и увеличения температуры плавления металл смешивают с медью, алюминием, оловом, магнием и свинцом.
Самым известным и востребованным сплавом является латунь. Это смесь меди с добавлением цинка, иногда встречаются и олово, никель, марганец, железо, свинец. Плотность латуни достигает 8700 кг/м 3 . Температура, нужная для плавления, держится на отметке 880 C о — 950 C о : чем больше в ней содержание цинка, тем она ниже. Сплав отлично сопротивляется неблагоприятной внешней среде, хоть и чернеет на воздухе, если не покрыта лаком, прекрасно полируется и сваривается контактной сваркой.
Существует два вида латуни:
- Альфа-латунь: более пластична, хорошо гнется в любом состоянии, но сильнее изнашивается.
- Альфа+бета-латунь: деформируется только при нагревании, при этом более износостойка. Часто сплавляют с магнием, алюминием, свинцом и железом. Это позволяет увеличить прочность, но уменьшает пластичность.
Сплав Zamak или Zamac состоит из цинка, алюминия, меди и магния. Само название образовано из первых букв латинских названий: Zink — Aluminium — Magnesium — Kupfer / Cuprum (Цинк-Алюминий-Магний-Медь). В СССР сплав был известен как ЦАМ: Цинк-Алюминий-Медь. Активно применяется в литье под давлением, плавление начинается при низкой температуре (381 C о — 387 C о ) и имеет низкий коэффициент трения (0,07). Обладает повышенной прочностью, что позволяет получать изделия сложной формы, которые не боятся сломаться: дверные ручки, клюшки для гольфа, затворы огнестрельного оружия, строительную фурнитуру, застежки разных видов и рыболовные снасти.
Читать также: Магнитный станок для сверления металла
Небольшой процент цинка (не более 0,01%) содержится в гартовых сплавах, применяемых в полиграфии для отливки типографских шрифтов и линеек, печатных форм и машинного набора. Это устаревшие смеси, на место которых пришел чистый цинк с небольшим добавлением примесей.
Невысокая температура, которая требуется для плавления цинка, часто компенсируется за счет сплавов с другими металлами, но бывает и наоборот. Если температура, необходимая для плавления «чистого» металла, составляет 419,5 C о , то сплав с оловом снижается до 199 C о , а с оловом и свинцом — до 150 C о . И хотя такие сплавы можно паять и варить, чаще всего смеси с цинком применяют только для заделки имеющихся дефектов из-за их слабой прочности. Например, сплав олова, свинца и цинка рекомендуется применять только на никелированных изделиях.
Чаще всего цинковые сплавы применяют для создания карбюраторов, рам спидометров, радиаторных решеток, гидравлических тормозов, насосов и декоративных элементов, деталей для стиральных машин, миксеров и кухонного оборудования, часовых корпусов, пишущих машинок, кассовых аппаратов и бытовой техники. Эти детали нельзя применять в промышленном производстве: при повышении температуры до 100 C о прочность изделия снижается на треть, а твердость — почти на 40%. При понижении температуры до 0 C о цинк становится слишком хрупким, что может привести к поломке.
Признаки дефицита
Недостаток цинка в организме может быть обусловлен рядом причин: недостаточное поступление с пищей, плохое усвоение, нарушения в работе щитовидной железы, заболевания печени. Кроме того, поводом для дефицита этого макроэлемента может стать переизбыток белков, фитина и селена, употребляемых с продуктами питания. Причиной данной проблемы и снижения качества жизнедеятельности в целом также могут стать моральные и физические нагрузки, нестабильный образ жизни, стрессовые ситуации, вредные привычки.
Перерасход цинка в организме происходит при воспалениях и онкологии. Причина в том, что при лечении данных заболеваний, активируется рост клеток, в котором важную роль играет цинк.
Кроме перечисленных выше причин, дефицит цинка может быть вызван такими факторами:
- Интенсивное потоотделение.
- Злоупотребление алкоголем.
- Восстановление после операции.
- Парентеральное питание.
- Прием большой дозы мочегонных, костикостероидных средств и эстрогенов.
- Передозировка медью, кадмием, свинцом и ртутью.
- Наличие паразитов в кишечнике.
Краткая история открытия элемента
Что такое цинк, люди знали еще до нашей эры. Ведь именно тогда научились применять сплавы, содержащие этот металл. Египтяне использовали руды, содержащие медь и цинк, сплавляли их и получали очень прочный, устойчивый к окислению материал. Были найдены предметы быта, посуда, выполненные из этого материала.
Название zinc встречается в трудах врача Парацельса в XVI веке нашей эры. В этот же период металл активно начинают использовать китайцы, отливая из него монеты. Постепенно знания об этом веществе и его хороших технических свойствах переходят в Европу. Тогда и в Германии, Англии также узнали, что такое цинк и где его можно использовать.
Латунь была одним из первых и самых известных сплавов, используемых еще с древних веков на Кипре, а позже в Германии и других странах.
Название происходит от латинского zincum, однако этимология не совсем ясна. Есть несколько версий.
- От немецкого zinke, что переводится как «острие».
- От латинского zincum, что означает «белый налет».
- Персидский «ченг», то есть камень.
- Древнегерманский zinco, что переводится, как «налет», «бельмо на глазу».
Сегодняшнее название элемент получил только в начале XX века. О значении ионов цинка в организме человека также стало известно лишь сравнительно недавно (XX век). До этого никакие недуги с этим элементом не связывали.
Однако известно, что уже в древности многие народы использовали супы из мяса молодого барашка как средство восстановления после болезни и для скорейшей поправки. Сегодня можно сказать, что эффект достигался за счет ионов цинка, которых в этом блюде содержится достаточно много. Он помогал восстановлению кровообращения, снятию усталости и активизировал мозговую деятельность.

Восстановитель
Цинк является хорошим восстановителем, поэтому он теряет свои электроны, чтобы их могли получить другие вещества; особенно катион металла. В форме порошка его восстанавливающее действие даже быстрее, чем у твердых гранул.
Он используется в процессах получения металлов из минералов; такие как родий, серебро, кадмий, золото и медь.
Аналогичным образом, его восстанавливающее действие используется для уменьшения количества органических веществ, которые могут быть задействованы в нефтяной промышленности, таких как бензол и бензин, или в фармацевтической промышленности. С другой стороны, цинковая пыль также находит применение в щелочных батареях из диоксида цинка и марганца.
Свойства цинка (таблица): температура, плотность, давление и пр.:
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Цинк |
| 102 | Прежнее название | |
| 103 | Латинское название | Zincum |
| 104 | Английское название | Zinc |
| 105 | Символ | Zn |
| 106 | Атомный номер (номер в таблице) | 30 |
| 107 | Тип | Металл |
| 108 | Группа | Амфотерный, переходный, цветной металл |
| 109 | Открыт | Известен с глубокой древности |
| 110 | Год открытия | до 1000 года до н. э. |
| 111 | Внешний вид и пр. | Хрупкий металл голубовато-белого цвета |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,0078 % |
| 120 | Содержание в морях и океанах (по массе) | 5,0·10-7 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,00003 % |
| 122 | Содержание в Солнце (по массе) | 0,0002 % |
| 123 | Содержание в метеоритах (по массе) | 0,018 % |
| 124 | Содержание в организме человека (по массе) | 0,0033 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 65,38(2) а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 |
| 203 | Электронная оболочка | K2 L8 M18 N2 O0 P0 Q0 R0
|
| 204 | Радиус атома (вычисленный) | 142 пм |
| 205 | Эмпирический радиус атома* | 135 пм |
| 206 | Ковалентный радиус* | 122 пм |
| 207 | Радиус иона (кристаллический) | Zn2+ 74 (4) пм,
88 (6) пм, 104 (8) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 139 пм |
| 209 | Электроны, Протоны, Нейтроны | 30 электронов, 30 протонов, 35 нейтронов |
| 210 | Семейство (блок) | элемент d-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 12-ая группа (по старой классификации – побочная подгруппа 2-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | -2, 0, +1, +2 |
| 302 | Валентность | II |
| 303 | Электроотрицательность | 1,65 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 906,4 кДж/моль (9,394197(6) эВ) |
| 305 | Электродный потенциал | Zn2+ + 2e– → Zn, Eo = -0,763 В |
| 306 | Энергия сродства атома к электрону | 0 кДж/моль |
| 400 | Физические свойства | |
| 401 | Плотность* | 7,14 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 6,57 г/см3 (при температуре плавления 419,53 °C и иных стандартных условиях, состояние вещества – жидкость),
6,4 г/см3 (при 800 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | 419,53 °C (692,68 K, 787,15 °F) |
| 403 | Температура кипения* | 907 °C (1180 K, 1665 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 7,32 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 115 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость* | 25,47Дж/(K·моль) |
| 411 | Молярный объём | 9,2 см³/моль |
| 412 | Теплопроводность | 116 Вт/(м·К) (при стандартных условиях), 116 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
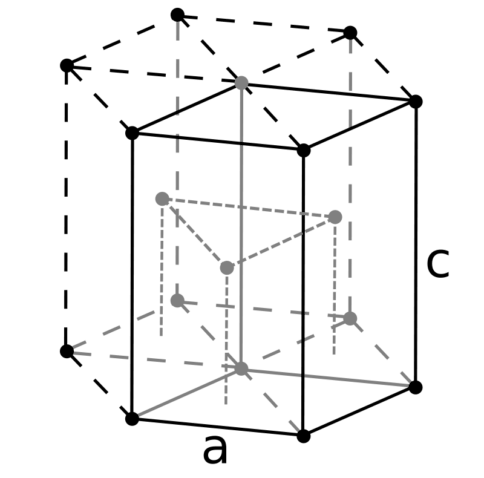
| 512 | Структура решётки | Гексагональная плотноупакованная
|
| 513 | Параметры решётки | a = 2,6648 Å, c = 4,9468 Å |
| 514 | Отношение c/a | 1,856 |
| 515 | Температура Дебая | 234 K |
| 516 | Название пространственной группы симметрии | P63/mmc |
| 517 | Номер пространственной группы симметрии | 194 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-66-6 |
Примечание:
205* Эмпирический радиус атома цинка согласно и составляет 134 пм и 138 пм соответственно.
206* Ковалентный радиус цинка согласно и составляет 122±4 пм и 125 пм соответственно.
401* Плотность цинка согласно и составляет 7,133 г/см3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело), согласно составляет 6,59 г/см3 (при 500 °C и иных стандартных условиях, состояние вещества – жидкость).
402* Температура плавления цинка согласно и составляет 419,6 °С (692,75 K, 787,28 °F) и 419,5 °С (692,65 K, 787,1 °F).
403* Температура кипения цинка согласно и составляет 906,2 °С (1179,35 K, 1663,16 °F) и 906 °C (1179,15 К, 1662,8 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) цинка согласно и составляет 7,28 кДж/моль и 7,24 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) цинка согласно и составляет 114,8 кДж/моль и 115,3 кДж/моль соответственно.
410* Молярная теплоёмкость цинка согласно составляет 25,4 Дж/(K·моль).
Где применяется
Свойства металла, его сплавов, соединений обусловили их использование в металлургии, электротехнике, медицине.
Чистый металл
Основные направления:
- Отрицательный электрод батареек, аккумуляторов.
- Восстановитель благородных металлов.
- Защитное покрытие стали от коррозии.
- Компонент твердых припоев для повышения легкоплавкости.
- Извлекатель металлов из чернового свинца.
До середины XX века популярной сферой применения цинка была полиграфия. Для создания черно-белых иллюстраций в газетах или книгах использовался метод цинкографии. На цинковой пластине кислотой вытравливалось изображение. Затем с нее на печатной машине делались оттиски.
 Слитки цинка
Слитки цинка
Сплавы
Цинк востребован как компонент сплавов с металлами. Например, латуни.
Она используется машиностроителями для точного литья:
- Автомобильная фурнитура.
- Оболочка карбюраторной коробки.
- Затворы травматических пистолетов.
Соединения
Применение нашли соединения металла, созданные природой или человеком:
- Хлорид – паяние металлов, изготовление фибры.
- Теллурид, селенид, фосфит – полупроводники.
- Селенид задействован при изготовлении специальных сортов стекла для лазеров.
- Окись – исходник для цинковых белил.
- Сульфид – компонент люминофоров (гибкие панели, экраны).
Фосфитом металла изничтожают грызунов.
Какой вид лома принимается, его чистота и требования к нему
Между тем, интерес скупщиков распространяется на такие категории этого металла:
«нулевые» или использованные заводские чушки;
разобранные или нет карбюраторы;
мебельная фурнитура любого плана (замочные разъемы, ручки, держатели), требуется строгое отделение от машиностроительных отходов.
Наиболее удобная форма сырья для изготовления изделий из Zn
Основная масса изделий, состоящая из этого металла, производится методами порошковой металлургии или обычным литьем. Поэтому цинковые заводские чушки, имеющие удобную форму для хранения, транспортировки, наиболее востребованный вид отходов металла. Чушки легко плавятся, перерабатываются в порошок. Отсюда и более высокая цена, чем у других форм.
Карбюраторы: разбирать или нет
Требования по чистоте металла иногда удивляют. Стальные тяги в радиаторах лучше удалить заранее и сдать, как отдельный вид сырья, иначе цена лома цинка уменьшается примерно на 25%. Это касается проводки, другого мусора, но здесь уже не возникает никаких противоречий.
История появления и утверждения химическим элементом
Точно неизвестно — кому, где и когда удалось впервые обнаружить цинк. Однако археологами обнаруживались цинковые сплавы в местах, относящихся к доисторическим временам. Достоверно известно – древние римляне производили медные монеты, состав которых включал это вещество, правда, с примесями.
Минуло почти тысяча лет, прежде чем люди начали использовать цинк в качестве металла как такового. Историки предполагают — впервые производство металла отметилось в Индии XIII века. Ещё спустя 300 лет, на территории Китая началось производство цинка в крупных масштабах.
Современная история начала производства цинка исчисляется от середины XVIII века. Первым 1737 году разработал и запатентовал процесс производства чистого цинка английский металлург Уильям Чампион. Производство в огромных промышленных масштабах осуществлялось путём плавки каламина древесным углем.
Между тем вещество окончательно было признано химическим элементом в 1746 году, благодаря усилиям немецкого химика по имени Андреас Сигизмунд Маргграф. Немецкий учёный использовал методы, подобные тем, что использовал Чемпион, с целью детального изучения цинка в стенах лаборатории.
Производство цинка
Как было сказано выше, чистого вида данного элемента в природе нет. Он добывается из иных пород, таких как руда – кадмий, галлий, минералы – сфалерит.
Металл получают на заводе. Каждый завод имеет свои отличительные особенности производства, поэтому оборудование для получения чистого материала различно. Оно может быть таким:
- Роторы, расположенные вертикально, электролитные.
- Специальные печи с достаточно высокой температурой для обжига, а также специальные электропечи.
- Транспортёры и ванны для электролиза.
В зависимости от принимаемого метода добычи металла, задействовано соответствующее оборудование.
Что такое цинк
Понятие и особенности
Для начала вашему вниманию предлагается общая характеристика цинка. Этот продукт является не только необходимым производственным металлом, но и важным биологическим элементом. В любом живом организме он присутствует до 4 % от всех элементов.Самые богатые месторождения цинка это Боливия, Иран, Казахстан и Австралия. В нашей стране одним из крупных производителей считается предприятие ОАО «ГМК Дальполиметалл».
Если рассматривать цинк со стороны периодической системе Менделеева, то он относится к переходным металлам и имеет следующие характеристики:
- Номер по порядку: 30
- Масса: 65,37.
- Степень окисления — +2.
- Цвет: синевато-белый.
Если рассматривать цинк со стороны простого вещества, то этот материал имеет следующие характеристики:
- Вид материала – металл.
- Цвет – серебристо-голубой.
- Покрытие – защищен оксидной пленкой, под которой скрывается блеск и сияние.
Цинк содержится в коре земли. Доля металла в ней не очень большая: всего 0,0076%.
Как единичного материала цинка не существует. Он входит в состав многих руд и минералов.
- Наиболее распространенными являются: цинковая обманка, клейофан, марматит. Кроме этого, цинк можно встретить в следующих природных материалах: вюртцит, франкленит, цинкит, смитсонит, каламин, виллемит.
- Спутниками цинка обычно являются: германий, кадмий, таллий, галлий, индий, кадмий.
- Наиболее популярными являются сплавы цинка и алюминия, меди, олова, никеля.
О роли цинка в нашей жизни расскажут специалист в этом видео:
Металлы-конкуренты
С цинком могут конкурировать только 4 металла: титан, алюминий, хром и медь. Описанные материалы имеют следующие характеристики:
- Алюминий: серебристо-белый цвет, хорошо проводит электричество и тепло, поддается обработке давлением, устойчив к коррозии, имеет низкую плотность, применяется в процессе производства стали (для повышения жаростойкости).
- Титан: серебристо-белый цвет, большая температура плавления, при соприкосновении с воздухом окисляется, низкая теплопроводность, легко поддается ковке и штамповке, при высокой температуре на поверхности образуется прочная защитная пленка.
- Хром: синевато-блестящий цвет, высокая твердость, хрупкость, стойкость к окислению в условиях атмосферы и воды, используется для декоративного покрытия.
- Медь: красный металл, имеет высокую пластичность, хорошую электропроводность, высокую теплопроводность, стойкость к коррозионным процессам, применяется в кровельных материалах.
Для строительных целей наиболее часто (кроме цинка) применяют и другие цветные металлы. К ним относятся: бронза, латунь, силумин, баббит, дюралюминий и несколько других.
Плюсы и минусы
Плюсы:
- Хорошая жидкотекучесть, благодаря чему легко заполняются литейные формы.
- Высокая пластичность во время проката.
- Чистый цинк хорошо поддается ковке.
- Благодаря своим свойствам и воздействию температуры способен принимать различные состояния.
- Отлично защищает изделие от коррозии, благодаря чему охотно пользуется спросом в строительстве и машиностроении.
- При нагреве вместе с фосфором или серой может взорваться.
- На воздухе теряет блеск.
- При комнатной температуре имеет маленькую пластичность.
- Не находится в природе в чистом виде.
Масса, механические, химические и физические свойства цинка, его основные характеристики будут рассмотрены нами ниже.
Получение
| Этот раздел не завершён.
Вы поможете проекту, исправив и дополнив его. |
Цинк в природе как самородный металл не встречается.
Цинк добывают из полиметаллических руд, содержащих 1—4 % Zn в виде сульфида, а также Cu, Pb, Ag, Au, Cd, Bi. Руды обогащают селективной флотацией, получая цинковые концентраты (50—60 % Zn) и одновременно свинцовые, медные, а иногда также пиритные концентраты. Цинковые концентраты обжигают в печах в кипящем слое, переводя сульфид цинка в оксид ZnO; образующийся при этом сернистый газ SO2 расходуется на производство серной кислоты. Чистый цинк из оксида ZnO получают двумя способами. По пирометаллургическому (дистилляционному) способу, существующему издавна, обожжённый концентрат подвергают спеканию для придания зернистости и газопроницаемости, а затем восстанавливают углём или коксом при 1200—1300 °C: ZnO + С = Zn + CO. Образующиеся при этом пары металла конденсируют и разливают в изложницы. Сначала восстановление проводили только в ретортах из обожжённой глины, обслуживаемых вручную, позднее стали применять вертикальные механизированные реторты из карборунда, затем — шахтные и дуговые электропечи; из свинцово-цинковых концентратов цинк получают в шахтных печах с дутьём. Производительность постепенно повышалась, но цинк содержал до 3 % примесей, в том числе ценный кадмий. Дистилляционный цинк очищают ликвацией (то есть отстаиванием жидкого металла от железа и части свинца при 500 °C), достигая чистоты 98,7 %. Применяющаяся иногда более сложная и дорогая очистка ректификацией даёт металл чистотой 99,995 % и позволяет извлекать кадмий.
Основной способ получения цинка — электролитический (гидрометаллургический). Обожжённые концентраты обрабатывают серной кислотой; получаемый сульфатный раствор очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу в ваннах, плотно выложенных внутри свинцом или винипластом. Цинк осаждается на алюминиевых катодах, с которых его ежесуточно удаляют (сдирают) и плавят в индукционных печах. Обычно чистота электролитного цинка — 99,95 %, полнота извлечения его из концентрата (при учёте переработки отходов) — 93—94 %. Из отходов производства получают цинковый купорос, Pb, Cu, Cd, Au, Ag; иногда также In, Ga, Ge, Tl.
Ссылки
- Шивер и Аткинс. (2008). Неорганическая химия. (Четвертый выпуск). Мак Гроу Хилл.
- Википедия. (2019). Цинк. Получено с: en.wikipedia.org
- Майкл Пилгаард. (2016, 16 июля). Цинк: химические реакции. Получено с: pilgaardelements.com
- Национальный центр биотехнологической информации. (2019). Цинк. База данных PubChem. CID = 23994. Получено с: pubchem.ncbi.nlm.nih.gov
- Воджес Райан. (25 июня 2019 г.). Свойства и использование металлического цинка. Получено с: thebalance.com
- Г-н Кевин А. Будро. (н.д.). Цинк + сера. Получено с: angelo.edu
- Алан В. Ричардс. (12 апреля 2019 г.). Обработка цинка. Encyclopdia Britannica. Получено с: britannica.com
- Металлы цинка чистоты. (2015). Промышленные приложения. Получено с: purityzinc.com
- Нордквист, Дж. (5 декабря 2017 г.). Каковы преимущества цинка для здоровья? Медицинские новости сегодня. Получено с: medicalnewstoday.com
Промышленное использование
Металлический цинк нашел широкое применение в промышленности. С его помощью, путем подземного выщелачивания добывают золото и серебро. Также цинк используется для защиты стали от коррозии (оцинковка и металлизация). В батарейках и аккумуляторах данное вещество выступает в качестве материала для отрицательных электродов.
Цинковые пластины широко используют в полиграфии, главным образом для печати иллюстраций. Из меди и цинка делают латунь. Сплавы этого вещества с магнием и алюминием нашли широкое применение в машиностроении. Цинк вводят в состав твердых припоев, для снижения температуры их плавления. Его окись является антисептическим и противовоспалительным средством, поэтому пользуется популярностью в медицине. Также с ее помощью производят краски – так называемые цинковые белила.

Селенид, фосфид, сульфид и теллурид цинка являются широко применяемыми полупроводниками. Кроме того, фосфид используется в составе отравы для грызунов, сульфид – в составе люминофоров, а селенид – в изготовлении оптических стекол.
Удельная теплота плавления
1. Даны графики зависимости температуры от времени двух тел одинаковой массы.
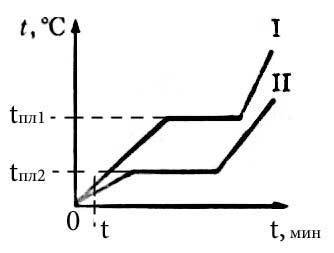
Графики состоят из трех участков: нагревание твердого тела, плавление тела (горизонтальный участок) и наггревание расплавленного тела. а) У какого тела выше температура плавления? Плавление происходит при неизменной температуре плавления (горизонтальный участок графика). По графику видно, что у первого тела температура плавления выше, чем у второго тела. б) У какого тела больше удельная теплота плавления? По графику видно, что горизонталный участок (время полного плавления тела) длиннее у второго тела Формула для плавления: Q = λm При одинаковой массе второе тело для полного плавления требует большего времени. За большее время ему подводится для плавления большее количество теплоты, чем первому телу. Но это воможно только, если удельная теплота плавления второго тела (λ) больше, чем удельная теплота плавления (λ) у первого тела. в) Одинаковы ли удельные теплоёмкости тел? Формула для нагревания: Q = cm (t2 — t1) За время t при нагревании обоим телам передается одинаковое количество теплоты: Q1= Q2 с1m1(t1-0) = c2m2(t2-0) c1m1t1 = c2m2t2 Но массы тел одинаковы. Тогда c1t1 = c2t2 Температура первого тела оказывается выше, чем второго. Это возможно, если с1< с2 Итак, удельная теплоемкость больше у второго тела, т.к. за одно и то же время второе тело нагревается меньше. 2. Тающий лёд принесли в помещение, температура которого 0 °С. Будет ли лёд в этом помещении продолжать таять?
Нет, не будет. Как известно, процесс плавления вещества (в данном случае таяния льда) возможен лишь при поглощении веществом какого-то количества тепла. Для дальнейшего таяния необходим подвод тепла, а если температура льда и температура в помещении одинакова, то это невозможно. Теплообмен воможен только при разной температуре веществ. Лед будет оставаться в таком же состоянии, как был, когда его внесли в помещение.
3. В ведре с водой плавают куски льда. Общая температура воды и льда 0 °С. Будет ли лёд таять или вода замерзать? От чего это зависит? Все будет зависеть от температуры окружающего воздуха. Если температура воздуха будет выше 0°С, то лед будет таять. Если температура воздуха будет ниже 0°С, то вода начнет замерзать. 4. Сколько энергии нужно затратить, чтобы расплавить лёд массой 4 кг при температуре О °С?

5. а) Сколько энергии требуется затратить, чтобы расплавить свинец массой 20 кг при температуре плавления? б) Сколько энергии понадобится для этого, если начальная температура свинца 27 °С?

Назад в «Оглавление»
Способы оцинкования
Металлы ржавеют в воде, влажном воздухе. Для решения этой проблемы их покрывают защитным слоем. Самый распространенный материал – цинк. Попутно обеспечивается защита от воздействия тока и химикалий.
Слой металла наносят несколькими способами.
Холодный
Применяется на любых материалах, кроме сплавов магния и высокопрочной стали.
Поверхность очищают от пыли, грязи, ржавчины, окалины. Наносят состав для холодной цинковки.
Горячий
Образец очищается, моется, протравливается, погружается в ванну с расплавленным цинком. На поверхности формируется покрытие в 0,035-0,097 мм.
Гальванический
На очищенную поверхность способом электролиза наносится слой цинка. Электролитом служит водно-цинковая среда.
Воздействие постоянного тока на поверхность заготовки (катод) осаждает ионы цинка (выделяются электролитом). Анодом выбирают цинковый материал.
Технология позволяет создавать слой 0,005 – 0,5 мм.
Преимущества метода:
- Высокая производительность.
- Низкая себестоимость.
- Равномерность покрытия.
- Работа с формами любой структуры, включая пористую.
- Создание декоративной оцинковки.
Эти характеристики сделали метод самым востребованным.
Минусы: губительность для экологии, хрупкость изделия при нарушении технологии.
Газотермический
Струя цинковой взвеси напыляется на поверхность изделия под углом.
Минусы:
- Неравномерность толщины слоя.
- Сложность контроля процесса.
- Дороговизна (втрое-вчетверо) по сравнению с другими способами.
Плюс: годится для обработки изделий любых форм, габаритов. Термодиффузионный
Реторту с шихтой и образцами помещают в камеру, снабженную индуктором. Тепло от реторты, изделий нагревает шихту.
В магнитном поле индуктора в изделиях образуются токи, нагревающие их за полчаса до 500-800°C.
Результат: 98% верхнего слоя покрытия – чистый цинк.
Толщина металлического слоя при термодиффузионном способе определяется параметрами изделий, шихты, временем прогрева, температурой.
Месторождения и получение
Самородного цинка в природе не существует. Сегодня используется около 70 минералов, из которых его выплавляют. Самый известный — сфалерит (цинковая обманка), который содержится в незначительных количествах в организме человека и животных, а также в некоторых растениях. Больше всего — в фиалке.
Цинковые минералы добывают в Казахстане, Боливии, Австралии, Иране, России. Лидеры по производству — Китай, Австралия, Перу, США, Канада, Мексика, Ирландия, Индия.
На сегодняшний день самый популярный метод получения чистого металла — электролитический. Чистота получаемого металла почти стопроцентная (возможны лишь небольшие примеси в объёме не более нескольких сотых процента. В целом они незначительны, поэтому такой цинк считается чистым).
Общее производство цинка во всём мире оценивается примерно в более чем десять миллионов тонн в год.