Выщелачивание
Выщелачивание наиболее примечательно тем, что позволяет получить металл даже из породы с низким содержанием золота или уже переработанной. Его принцип действия состоит в следующем:
- Добытая золотая порода дробится на мелкие частицы, размерами не больше песчинки.
- В полученную смесь добавляют цианистый раствор и размешивают. Из полученной смеси цианид высвобождает золото из породы и примесей.
- Жидкость откачивается, а твердые частицы отправляют в специальный резервуар, где остатки цианистого раствора отделяет остатки золота. Тяжелые частицы оседают.
- В раствор же добавляют цинк, запуская процесс «цианистого выщелачивания», который позволяет вычленить до 98% золота. Достаточно затратный, но и окупаемый метод.
Однако на этом процесс еще не заканчивается. Для последующей очистки золото отправляют в печь, предварительно смешав со специальной химической смесью – флюсом. Нагревается до температуры в 1500 С°. В результате получают благородный металл с 80%-й очисткой от примесей.

История
Уильям Волластон (1766—1828)
В 1803 году известный лондонский торговец минералами Форстер получил анонимное письмо с просьбой попытаться продать небольшое количество нового химического элемента — «палладия», слиток которого прилагался к письму
Таинственный металл был выставлен на продажу и привлёк всеобщее внимание. Среди английских химиков разгорелись споры, является ли этот металл действительно новым химическим элементом или же это просто сплав уже ранее известных металлов
Химик Ричард Ченевикс, желая разоблачить «мошенническую подделку», купил слиток «палладия». Вскоре Ченевикс выступил с докладом перед членами Лондонского Королевского общества, где объявил, что данный металл — всего лишь сплав платины с ртутью. Однако секретарь Королевского общества химик Уильям Хайд Волластон публично усомнился в выводах Ченевикса. Другим химикам не удалось выделить в этом «сплаве» ни платины, ни ртути. Споры вновь обострились и какое-то время активно продолжались. Когда же они стали стихать, в научном журнале Nicholson’s Journal появилось анонимное объявление, что любому, кто в течение года сможет изготовить искусственный палладий, будет выплачена награда в 20 фунтов стерлингов. Интерес к металлу вновь подскочил, но никому так и не удалось его изготовить.
В 1804 году Уильям Волластон доложил Королевскому обществу, что в платиновой руде из Южной Америки он обнаружил новые ранее неизвестные металлы — палладий и родий. Стремясь очистить выделенную из руды «сырую» платину от примесей золота и ртути, он растворял её в царской водке, а затем осаждал её из раствора нашатырём. Оставшийся раствор имел розовый оттенок, что было невозможно объяснить присутствием золота и ртути. Тогда в этот раствор был добавлен цинк, что привело к выпадению чёрного осадка. Волластон обнаружил, что если попытаться растворить этот высушенный осадок царской водкой, то часть его растворяется, а часть — нет. После разбавления раствора водой Волластон добавил в него цианид калия, что привело к обильному выпадению осадка уже оранжевого цвета, который при нагревании сначала приобрёл серый цвет, а затем сплавился в капельку металла — палладия, который по удельному весу был меньше ртути. Из оставшейся нерастворённой части чёрного осадка им был выделен другой металл — родий.
Лишь в феврале 1805 года в Nicholson’s Journal было опубликовано открытое письмо Волластона, в котором он признался, что скандальная шумиха вокруг палладия — дело его рук. Именно он пустил в продажу новый металл, и он же дал анонимное объявление с обещанием премии за его искусственное изготовление, уже располагая доказательством, что палладий — это новый металл.
Керамические конденсаторы
Для проведения аффинажа необходимо подготовить дорогостоящие компоненты и соответствующую посуду. Поэтому во избежание дополнительных расходов, рекомендуется перед началом работы подготовить достаточное количество исходных материалов, в составе которых присутствует много палладия.
В современной электронике содержание этого материала невелико. И чтобы получить металл в относительно большом объеме, следует запастись необходимым количеством керамических конденсаторов: КМ-3, КМ-4, КМ-5 и КМ-6. Именно они, по мнению специалистов, соответствуют приведенным выше условиям. Однако керамические конденсаторы стоят дорого.
Найти КМ можно в электронике, выпущенной в советское время. Керамические конденсаторы ранее использовались в:
- аналоговой технике;
- компьютерах;
- генераторах;
- измерительных устройствах (Е7-14, Р2-73);
- осциллографах (C-114, 116 и другие) и так далее.
Домашние методы определения подлинности палладия
В домашних условиях можно определить, какой металл перед вами находится, даже не имея в запасе глубоких познаний в физике и химии или дорогостоящего оборудования в кустах.
Так, если вы приобрели на блошином рынке кольцо безо всяких опознавательных знаков, и продавец упорно уверял, что это белое золото, есть несколько способов определить, действительно ли в украшении содержится палладий, или это сплав никеля. Итак, как проверить, какой перед нами металл?
По весу и плотности
Метод простой и быстрый. Но понадобятся достаточно точные весы – с погрешностью до одной сотой грамма. И дистиллированная вода, ее достать легко в любой аптеке или автомагазине.

Что я делала, чтобы определить, из чего сделано мое кольцо:
- Взвешиваю сухое украшение – 3,12 г.
- Наливаю в стакан дистиллированную воду, ставлю его на платформу весов и взвешиваю. Масса стакана с водой – 172,21 г. Если весы с функцией обнуления – этот этап можно пропустить, просто обнулив показания весов.
- Подвешиваю кольцо на нитке и полностью погружаю его в стакан с водой так, чтобы изделие не касалось дна или стенок.
- Фиксирую взвешенный результат – 172,48 г.
- Разница между массами приравнивается к объему кольца. 172,48-172,21=0,27 см3.
- Высчитываю плотность изделия: 3,120/0,27=11,56 г/см3.
- Смотрю в интернете таблицу плотностей металлов. В диапазоне от 8 до 12 находятся несколько подходящих:
- серебро – 10,49;
- палладий – 12,02;
- никель – 8,96.
Учитывая, что ювелирный сплав палладия содержит обычно серебро и никель, делаю вывод, что кольцо мое – палладиевое, причем достаточно высокой пробы. Нельзя не порадоваться, определив подобную ценность.
С помощью азотной кислоты
Палладий – единственный из драгоценных металлов платиновой группы, который растворяется в азотной кислоте, поэтому по реакции на небольшую каплю реактива можно определить, какой сплав перед нами.

Если поверхность исследуемого металла окрасится в красноватый оттенок, можно с уверенностью сказать, что перед нами палладий. Отмечу, что при работе с кислотами стоит быть предельно осторожным и использовать средства защиты.
С помощью пробирного камня
Пробирный камень — сланцевая или яшмовая пластина черного цвета с набором игл из драгметаллов для проведения пробы. Из набора выбираем наиболее подходящую по цвету к исследуемому металлу иглу и чертим линию на пробирном камне. Затем зачищаем небольшой участок нашего изделия и чертим им на пробирном камне такую же полоску.

После чего концентрированной азотной кислотой проводим линию поперек начерченных, оставляем до полного высыхания и сравниваем по цвету действие реагента. Если окраска образца совпадает с пробой, значит, удалось определить именно драгоценный металл.
Соль
Соль также придет на помощь, если необходимо проверить подлинность украшения. Для этого эксперимента придется немного потрудится. Понадобится:
- жестяная банка;
- батарейки;
- раствор соли с водой.
В банку налейте раствор и в него положите украшение. Плюс батарейки необходимо подключить к изделию, а минус – к банке. В случае выпадения осадка и помутнения жидкости вы имеете дело с подделкой. Если вода осталась чистой, все в порядке. Если запахло хлором, не пугайтесь. Это результат реакции. У вас в руках оригинал.
С помощью йодистого калия и царской водки
Метод достаточно трудоемкий и требует мер предосторожности. Царская водка – это смесь соляной и азотной кислот в соотношении 1:3
Вещество прекрасно растворяет все драгоценные металлы, именно с ее помощью определяют их наличие в сплаве. Поскольку нас интересует палладий, добавлю, что осадить его из раствора можно, добавив йодид калия. Процесс хорошо показан в видео.
Проверка на подлинность при помощи магнита
Каждый человек сможет найти у себя дома магнит. С его помощью также можно проверять золотые изделия на подлинность.
В процессе эксперимента магнит необходимо поднести к предполагаемому золотому аксессуару. Если он прилипнет к магниту, значит это сто процентов подделка! Настоящее золото высокой пробы не должно примагничиваться.
История
Уильям Хайд Волластон
Уильям Хайд Волластон отметил открытие нового благородного металла в июле 1802 года в своей лабораторной книге и назвал его палладием в августе того же года. Волластон очистил некоторое количество материала и предложил его, не называя первооткрывателя, в небольшом магазине в Сохо в апреле 1803 года. После резкой критики Ричарда Ченевикса за то, что палладий представляет собой сплав платины и ртути, Волластон анонимно предложил вознаграждение в размере 20 фунтов стерлингов. на 20 зерен синтетического сплава палладия . Ченевикс получил медаль Копли в 1803 году после публикации своих экспериментов с палладием. Волластон опубликовал открытие родия в 1804 году и упоминает некоторые из своих работ по палладию. Он сообщил, что он был первооткрывателем палладия в публикации 1805 года.
Он был назван Волластоном в 1802 году в честь астероида 2 Паллада , открытого двумя месяцами ранее. Уолластон найдено палладия в сырой платиновой руды из Южной Америки путем растворения руды в царской водке , нейтрализации раствора гидроксида натрия , и осаждении платины , как хлороплатинат аммония с хлоридом аммония . Он добавил цианид ртути с образованием цианида палладия (II) , который нагревали для извлечения металлического палладия.
Одно время для лечения туберкулеза назначали хлорид палладия из расчета 0,065 г в день (примерно один миллиграмм на килограмм массы тела). Это лечение имело множество отрицательных побочных эффектов , и позже было заменено более эффективными лекарствами.
Чаще всего палладий используется в каталитических нейтрализаторах в автомобильной промышленности. В период до 2000 г. поставки палладия из России на мировой рынок неоднократно задерживались и прерывались; по политическим причинам экспортная квота не была предоставлена вовремя. Последовавшая паника на рынке привела к тому, что в январе 2001 года цена достигла рекордного уровня в 1340 долларов за тройскую унцию (43 доллара за г ). Примерно в то же время Ford Motor Company , опасаясь, что производство автомобилей будет остановлено из-за нехватки палладия, создала запасы металл. Когда в начале 2001 года цены упали, Ford потерял почти 1 миллиард долларов США.
Мировой спрос на палладий увеличился со 100 тонн в 1990 году до почти 300 тонн в 2000 году. По данным Геологической службы США, мировое производство палладия на рудниках в 2006 году составило 222 тонны . Многие были обеспокоены стабильными поставками палладия после аннексии Крыма Россией , отчасти потому, что санкции могут помешать российскому экспорту палладия; любые ограничения на экспорт палладия из России могли усугубить уже ожидавшийся большой дефицит палладия в 2014 году. Эти опасения подняли цены на палладий до самого высокого уровня с 2001 года. В сентябре 2014 года они превысили отметку в 900 долларов за унцию. Однако в 2016 году палладий стоил около 614 долларов за унцию, поскольку России удалось сохранить стабильные поставки. В январе 2019 года фьючерсы на палладий впервые в истории превысили 1344 доллара за унцию, в основном из-за высокого спроса со стороны автомобильной промышленности. 6 января 2020 года цена на палладий достигла 2024,64 доллара за тройскую унцию (65,094 доллара за г), впервые превысив отметку в 2000 долларов за тройскую унцию.
Применение палладия
Главной областью применения палладия является производство автомобильных катализаторов. По данным Johnson Matthey в автомобильной индустрии используется около 70% добываемого палладия. Около 10% используется в электронной промышленности для производства конденсаторов и электрических разъемов. По 5% палладия используется в химической промышленности, медицине и в качестве инвестиций. Оставшаяся часть используется в ювелирной промышленности и в других областях.
Палладий для ювелиров
За последние 10 лет использование палладия в ювелирной промышленности упало практически в 3 раза, при том что объемы добычи палладия увеличились примерно на 25% за тот же период. Причина, очевидно, заключается в росте цен на палладий в связи с возросшими потребностями автомобильной промышленности.
В ювелирном производстве палладий в основном используют как легирующий металл в сплавах золота и платины. Возросшие цены заставили производителей искать более дешевые альтернативы. Кроме того, спрос на ювелирные изделия, изготовленные из палладия, продолжает оставаться невысоким.
ВСЕ ЮВЕЛИРНЫЕ МЕТАЛЛЫ: КАТАЛОГ | ЮВЕЛИРНЫЕ МЕТАЛЛЫ — СПРАВОЧНИК | ДРАГОЦЕННЫЙ МЕТАЛЛ ПАЛЛАДИЙ
Свойства палладия | История палладия
Драгоценный металл золото | Драгоценный металл серебро | Драгоценный металл платина
Добыча и промышленное получение
Получение чистого металла выполняется в несколько этапов:
- Подготовка расходного сырья. Его нагревают в специальных фарфоровых котлах. В процессе нагревания котлы заполняются царской водкой.
- Переведение платины в осадок с использованием специальных фильтров. От основы отделяются присадки, сторонние компоненты, которые интересны для получения палладия.
- Обработка фильтрата. Проводится процедура аффинажа, в ходе которой получается труднорастворимое соединение, которое называется дихлордиаммином палладия.
- Очищение нужного металла от примесей.
- Прокаливание. Проводится в герметичных камерах, заполненных водородом.
Полученный губчатый палладий переплавляется в заготовки требуемых размеров и формы.
Добыча руды (Фото: Instagram / khabkrai)
Физические свойства
| Цвет минерала | белый |
| Цвет черты | стальной серый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 4.5-5 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 11.3 — 11.8 г/см3 |
| Радиоактивность (GRapi) | |
| Магнетизм | парамагнетик |
Электронная схема палладия
Порядок заполнения оболочек атома палладия (Pd) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
Палладий имеет 46 электронов, заполним электронные оболочки в описанном выше порядке:
Элемент Pd является исключением!
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
10 электронов на 4d-подуровне
Степень окисления палладия
Атомы палладия в соединениях имеют степени окисления 4, 2, 0.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
4+Pd 2+Pd
Pd 0
Валентность Pd
Атомы палладия в соединениях проявляют валентность IV, II.
Валентность палладия характеризует способность атома Pd к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Квантовые числа Pd
Квантовые числа определяются последним электроном в конфигурации, для атома Pd эти числа имеют значение N = 4, L = 2, Ml = -2, Ms = ½
Энергия ионизации
Чем ближе электрон к центру атома — тем больше энергии необходимо, что бы его оторвать. Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo. Если не указано иное, то энергия ионизации — это энергия отрыва первого электрона, также существуют энергии ионизации для каждого последующего электрона.
Соединим палладий с…
В разных странах свои предпочтения видам палладиевых сплавов.
Европейские и североамериканские ювелиры предпочитают работать со сплавом 950 пробы, в котором лигатурой служат медь или рутений. Российские ювелиры предпочитают сплав палладия с никелем или серебром (пробы 500 и 850), или палладий с медью (проба 850).
Внимание: выгодны обручальные кольца из палладия 950 пробы. Со временем пальцы становятся толще, раскатать палладиевые колечки до нужного размера легко
Проверить соответствие пробы заявленному в домашних условиях невозможно, это делается специалистами.
Рекомендуем: СЕРЕБРО — лунный металл от любой нечисти
Применение
Катализаторы
Палладий часто применяется как катализатор, в основном в процессе гидрогенизации жиров и крекинге нефти.
Хлорид палладия PdCl2 используется как катализатор и для обнаружения микроколичеств угарного газа в воздухе или газовых смесях.
Очистка водорода
Так как водород очень хорошо диффундирует через палладий, палладиевые мембраны применяют для глубокой очистки водорода. Также палладий способен исключительно эффективно обратимо аккумулировать водород. Для экономии дорогостоящего палладия при производстве мембран для очистки водорода и разделения изотопов водорода разработаны сплавы его с другими металлами (наиболее эффективен и экономичен сплав палладия с иттрием).
Гальванотехника
Хлорид палладия применяется в гальванотехнике, как активирующее вещество при гальванической металлизации диэлектриков — в частности, осаждении меди на поверхность слоистых пластиков при производстве печатных плат в электронике.
Электрические контакты
Палладий и сплавы палладия используется в электронике — для покрытий, устойчивых к действию сульфидов (преимущество перед серебром).
В частности, палладий постоянно расходуется для производства реохордов прецизионных сопротивлений высокой точности (военная и аэрокосмическая техника), в том числе в виде сплава с вольфрамом (например, ПдВ-20М). Применение в данных узлах обусловлено высокой износоустойчивостью палладия, что идеально подходит для его использования в контактных группах. К слову говоря, реохорды из палладиевой проволоки широко применялись и в аппаратуре гражданского назначения, а палладий в чистом виде применялся в контактах шаговых переключателей контрольно-самопишущих машин, в контактах и струнах МКС (многократных координатных соединителях) АТСК (автоматических телефонных станций координатных) производства с 1982 по 1987 года СССР.
Палладий входит также в состав керамических конденсаторов (тип КМ), с высокими показателями температурной стабильности ёмкости в высокочастотной аппаратуре радиовещания, радиосвязи, телевидения.
В ювелирном и монетном деле
Памятная монета «Иван III» достоинством в 25 рублей (СССР, 1989 год). Изготовлена из палладия 999 пробы.
- В сплавах, используемых в ювелирном деле (например, для получения сплава золото-палладий — так называемое «белое золото»). Палладий даже в небольшой концентрации в сплаве (около 1 %) изменяет цвет сплава на основе золота из жёлтого в серебристо-белый. Основные сплавы палладия с серебром, используемые в ювелирном деле, имеют пробы 500 и 850 по серебру (так как наиболее технологичны при механической обработке и декоративны).
- Из палладия иногда чеканятся памятные монеты ограниченным тиражом.
В медицине
- Из палладия и его сплавов изготавливают медицинские инструменты, детали кардиостимуляторов, зубные протезы;
- В некоторых странах незначительное количество палладия используется для получения цитостатических препаратов — в виде комплексных соединений, аналогично цис-платине.
- Бета-активный палладий-103 используется для брахитерапии в лечении онкозаболеваний.
Другие области применения палладия
- Для изготовления специальной химической посуды, стойких к коррозии деталей высокоточных измерительных приборов, прецизионных механических инструментов.
- Определённое количество палладия расходуется для изготовления химической аппаратуры для производства плавиковой кислоты (сосуды, перегонные кубы, детали насосов, реторты).
- Покрытия из палладия применяются для нанесения на электрические контакты для предотвращения искрения.
Примеры аффинажа
Аффинаж проводится различными методами. Для выделения материала дома оптимальным выбором станут:
- электролиз;
- последовательные химические реакции.
Для проведения электролиза потребуется высококонцентрированная серная кислота. Она замещает собой электролит. В качестве катода используется свинец, а анод – электродеталь, из которой выделяется требуемый материал. В процессе проведения процедуры исходные медные и латунные сплавы остаются нетронутыми. После электролиза выделяется палладий с различными примесями. Для их удаления металл помещается в соляно-азотную кислоту.
Перед началом процедуры в емкость, заполненную электролитом, подается напряжение 11-13 вольт. Воздействие электрического тока приводит к образованию в сосуде порошка или хлопьев. Именно в таком виде выделяется палладий.
Электролиз – это относительно простой способ получения металла. Добыть палладий посредством химической реакции сложнее, так как, в зависимости от состава сплава, подбираются исходные реагенты. Так, для отделения серебра и золота потребуются:
- азотная и соляная кислоты, в том числе и их смесь;
- аммиак.
Важно помнить о том, что в процессе получения палладия посредством химической реакции в окружающее пространство выделяется множество опасных для организма веществ. Перед началом процедуры рекомендуется надеть средства защиты (перчатки и маску) и создать условия для вентиляции помещения
Нахождение в природе и добыча
Добыча платины и палладия осуществляется на коренных и россыпных месторождениях. Чем они отличаются друг от друга? В коренных месторождениях металл входит в состав минералов и добывается как побочный продукт при обработке никелевых или медных руд. Рассыпные месторождения представляют собой разрешенные коренные залежи руды, где Pd высвободился и накопился в виде самородков.
Добыча палладия на россыпных месторождениях занимает около 2% от мирового производства объема элемента. Крупнейшие из них находятся в уральских и дальневосточных районах России, в Канаде, США, Австралии и Колумбии. Оставшиеся 98 % Pd извлекаются из недр земли на коренных месторождениях медно-никелевых, платиновых и хромовых руд.

Мировыми лидерами по добыче драгметалла на таких месторождениях являются Россия и ЮАР. Безоговорочное первое место среди добывающих предприятий отрасли занимает ГМК «Норильский никель», производящий более 40% мировых объемов Pd. Металлургический комбинат извлекает металл как побочный элемент при добыче основных своих продуктов – меди и никеля. Среди добывающих активов «Норильского никеля», имеющих потенциал запасов палладия, выделяются месторождения на полуострове Таймыр – Талнахское, Октябрьское и Норильск-1, а также на территории Кольского полуострова.

Следующим по значению источником металла в мире принято называть Бушвелдский комплекс, расположенный на территории Южно-Африканской Республики. Территория месторождения обладает крупнейшими запасами платиноидов в мире.
Pd в самородках имеет примеси других драгоценных металлов, но и сам часто является одним из элементов самородных золота или платины. При добыче палладия в Норильске геологами была обнаружена палладистая платина – соединение платины и ее «младшего брата» в отношении 60%/40%. Еще один подобный союз, на этот раз с золотом, был найден в Бразилии. Такое золото с 10%-м содержанием Pd получило название порпецит: от чистого желтого металла отличить его визуально также проблематично.
В составе каких минералов встречается палладий? Рассмотреть их можно на фото образцов. Самыми известными минералами, содержащими в своем составе Pd, являются палладит, станнопалладит, брэггит и потарит. Некоторые соединения даже на сегодняшний день не имеют названий, так как мало изучены в виду своей редкости.
Элемент Pd является компонентом не только недр нашей планеты, но и космических объектов: палладий содержится в железных и каменных метеоритах, прилетающих на Землю.

Как добывают, основные месторождения
В чистом виде палладий встречается редко, обычно его получают переработкой руд никеля, серебросодержащих руд, меди. Добывают Pd обычно там же, где и платину.
Процесс аффинажа на производстве происходит в несколько этапов:
- нагревание сырья вместе с царской водкой;
- фильтрование, отделение от примесей;
- получение дихлородиамминпалладия;
- восстановление водородом.
Металл получают промышленным способом, извлечение палладия в условиях домашней химической лаборатории считается довольно сложным делом из-за необходимости работать с опасными реагентами. Для получения Pd из сплава с серебром используют азотную кислоту, сплавы с золотом рекомендуется растворять царской водкой.

Из хлористого палладия делают палладиевую чернь – смесь металла с углеродом. Пористый древесный уголь пропитывают раствором палладия. Затем нагревают в присутствии водорода, после чего металл оседает на носителе. Черный порошок – «палладий на угле» или, как его еще называют, – «палладий на углероде» используется для ускорения реакции гидрогенизации (присоединение водорода к веществу).
Палладия по мировым запасам примерно вдвое больше, чем желтого драгметалла – золота. Основные залежи расположены в ЮАР и в России. Есть богатые месторождения и в Канаде. На первом месте по производству и добыче находится Россия (более сотни тонн в год) – палладий добывают в районе Норильска (Талнах). Почти половину всего палладия поставляет российский «Норникель». Крупное месторождение (пока не разрабатываемое) обнаружено в Мурманской области.
Основные факторы образования россыпного золота
Первичными являются коренные месторождения, образовавшиеся в результате бурных магматических процессов. Это трещины или расщелины в породе или залежах руды. Они всегда расположены в горной местности, появившейся на свет в ходе выхода магматической лавы на поверхность земли. В этих горных породах создаются рудники, в которых промышленным способом происходит добыча полезных ископаемых.
Золото россыпного типа является производным от коренного, так как это те же золотые частички, которые со временем под воздействием природных явлений откололись от основного массива и распространились далеко за пределы золотоносной жилы. На залежи воздействуют перепады температуры, грунтовые воды, жизнедеятельность микроорганизмов и другие факторы, из-за которых золотые частицы могут покинуть свое изначальное местоположение. Например, часто их вымывают из породы обильные дожди с сильными порывами ветра. С дождевыми потоками и талыми водами они вливаются в горные речки, где их затем и находят старатели.
Виды золотой россыпи
Специалисты выделяют следующие виды россыпного золота
| Разновидности | Характеристики |
| Террасовые россыпи. | Золотые россыпи распространяются по воде, а потому искать их нужно возле горных речек и в них самих. Террасовые золотые песчинки можно обнаружить на берегах водоемов. Они откладываются в результате разлива реки после обильных паводков и дождей. Песчинки золота имеют больший вес, чем простой ил, а потому сдвинуть их с места может бурное течение. Когда река разливается, то это происходит быстро и активно, а вот снижается уровень воды постепенно. Поэтому золотые песчинки не уплывают вместе с водой, а остаются на берегах. |
| Русловые. | Сильные наводнения происходят с разной регулярностью, а потому золото россыпного типа находится и на дне горных водоемов. Этот вид россыпей называется русловым. Чтобы отыскать его, старателям приходится вручную перемывать огромное количество осадочных отложений, которые они достают уз русел рек. |
| Аллювиальные. | Такие россыпи золота, как правило, появляются на склонах в остатках золотоносной руды. Под воздействием природных ил эти куски отбились от основного пласта залежей руды. Зачастую их находят неподалеку от разведанных и разрабатываемых месторождений. Под воздействием дождевой воды их может немного смыть, подальше отодвинув от изначального места, но все равно они будут относительно неподалеку. |
Но, интересно, что бывают случаи, когда аллювиальные россыпи находят на тех местах, где уже даже прекратил существование тот холм, с которого давным-давно они были смыты
Потому для золотодобытчиков очень важно иметь полную информацию относительно геологической истории исследуемой местности. Это касается и сведений о том, где пролегали горные потоки, которые со временем могли поменять свои пути
Добыча и использование
Палладий – это драгоценный металлический сплав, который входит в состав более 30 минералов. Встречается и в виде самородков. Большое количество элемента входит в золотые и серебряные сплавы.

Палладіумъ считается редким драгоценным металлом. Он встречается гораздо реже, чем золото. Среди основных мест добычи можно выделить:
- Норильскую платину. Она является важным месторождением элемента. Здесь более половины от всех минералов составляет палладий. Остальная часть – ртуть, медь, никель.
- Большое количество металла добывается в Бразилии. Здесь находят самородки с содержанием элемента более 10%.
Применение металла палладиум различно. Нет практически ни одной области, где бы он не использовался:
- Благодаря своим удивительным свойствам металл широко применяется в химической промышленности. Элемент способен поглощать количество водорода в 1000 раз больше количества самого металла. Поэтому он используется как катализатор, например, при производстве маргарина. Это позволяет устранить возможность попадания в продукт никеля.
- Применяют этот элемент и для удаления водорода из растворов и газовых смесей. Сделать это можно, установив в качестве мембраны миллиметровую пластину из палладия.
- Сплавы из металла не поддаются окислению даже под электрической дугой. Это позволило применять минерал в электротехнической индустрии. Например, титан с незначительным добавлением палладия значительно увеличивает устойчивость состава к возникновению химических реакций.
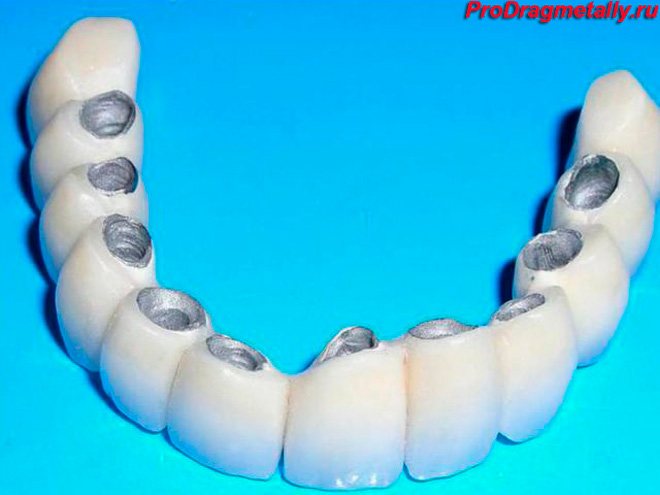
- Используется металл и в медицине, в частности, кардиологии, фармацевтике для производства ацетилена, в стоматологии для протезирования зубов. Элемент значительно снижает стоимость протезов, оставляя качество на высоком уровне.
- Применяют элемент и в промышленности – для производства труб. Металл может растягиваться до тех пор, пока нагрузка не составит 18,5 кг на 1 квадратный миллиметр. Добавляя родий с рутением, можно увеличить показатели сплава. Это позволяет создавать трубы без швов и спаек.
- Более 70% всей добычи минерала используется в машиностроении. Элемент применяется, как машинный катализатор, делая выхлопные газы более чистыми.
- Около 15% металла используется в электронной сфере производства.
- Всего 10% минерала применяется в ювелирном деле. Но данные сплавы высоко ценятся ювелирами. Наибольшую популярность имеет сплав с золотыми примесями, в результате чего получается золото, называемое белым. Благодаря своему мягкому блеску оно считается отличным окаймлением для бриллиантов.
Способы добычи
Работа с палладиевыми месторождениями ведется в двух формах:
- закрытая (шахтная);
- открытая (карьерная).
В первом случае для добычи драгметалла создается система подземных туннелей — шахт. В найденном рудном пласте создаются небольшие по размерам отверстия, в которые затем закладывается взрывчатка. Разрыхленный взрывом грунт обрабатывается механизированным или ручным способом для извлечения частиц палладия. По окончании первичной очистки руда переправляется на поверхность, а затем транспортируется к месту дальнейшей переработки.
Для работы во втором случае привлекается тяжелая землеройная техника и транспорт для перевозки извлеченной руды. С ее помощью разрабатывают грунтовый карьер, из которого затем извлекают палладий. Далее ее перевозят для переработки на соответствующие предприятия.






























