По типу мембраны, ионоселективные электроды подразделяют на следующие типы:
— Твердые электроды
— мембраны данного типа электродов представляют собой монокристаллы или
поликристаллы солей, труднорастворимых в воде. В таких мембранах, как правило,
один из двух составляющих соль ионов может под действием электрического поля
перемещаться в кристаллической решетке. Электроды с твердой мембраной – это
галогенсеребряные электроды, сульфидсеребряные электроды, лантафторидные
электроды, а также электроды на основе сульфидов или халькогенидов. Сюда же
относят стеклянные электроды.
— Жидкостные электроды
— в основе жидких мембран лежат растворы ионообменных веществ, таких, как жидкие
катиониты или аниониты, или же нейтральные хелатные
соединения в органических растворителях. При помощи пористых перегородок, такие
растворы отделяются от анализируемых растворов, при этом возникает разность
потенциалов;
— Газовые электроды – Газовый электрод
включает в себя основной ионоселективный электрод и вспомогательный
сравнительный электрод, которые контактируют с небольшим объемом
вспомогательного раствора, который отделяется от исследуемого раствора либо
газовой прослойкой, либо гидрофобной газопроницаемой мембраной. Премуществом
таких электродов является: долгий срок эксплуатации, быстрое время отклика
электрода, невосприимчивость к механическим помехам, благодаря чему можно
использовать электрод в потоке. Одним из наиболее распространенных жидкостных
электродов, является электрод для анализа содержания аммиака.
— Энзимные электроды
— действие энзимных электродов подобно
мембранным электродам, однако существенным их отличием является то, что вместо
мембраны, здесь используются энзимы, мобилизованные на индикаторной поверхности
электрода. От того, насколько высока концентрация энзимов в гелевом слое,
зависит эффективность применения таких электродов. Наибольшее распространение
энзимные электроды получили для определения содержания глюкозы и мочевины, а
также аминокислот.
Назначение и принцип работы
Обычно ионоселективные электроды – приборы, главным компонентом которых является мембрана. Ее особенность заключается в проницаемости только для определенного иона.
Установив мембрану между двумя растворами, создастся разность потенциалов, состоящая из потенциала диффузии и межфазных скачков. В результате содержание возможно определить по измерению электродвижущей силе гальванического элемента.
Данный компонент состоит из исследуемого и эталонного раствора. Искомое значение содержания ионов вычисляется по формуле.
 Стеклянный ионоселективный электрод.
Стеклянный ионоселективный электрод.
Стеклянные электроды в данном случае рассматриваются, как твердые электролиты. Их главной особенностью является участие в ионообменном взаимодействии с раствором.
Существуют устройства не только с твердой, но и с жидкой, а также пленочной мембраной. Селективность второго типа определяется комплексообразованием между мембраной и электролитическим раствором.
Конечно же, тот факт, что мембрана пропускает через себя только один конкретный тип иона, идеализирован. На самом деле она проницаема также и для других элементов, которые называются посторонними или мешающими.
Тем не менее избирательность к определяемому и мешающему иону у электрода различна. Этот параметр определяется так называемым коэффициентом селективности.
Таким образом, принцип работы основан на измерении потенциала внутримембранных межфазных скачков. Благодаря высокой селективности, данные устройства широко применяются в медицине, химии, для контроля загрязнения воздуха, анализа грунта и так далее.
Преимущества введения лекарства посредством электрофореза
Помимо электрофореза, лекарства в человеческий организм можно вводить и более стандартными путями – перорально (через рот) и инъекционно (путем осуществления внутривенного, подкожного, внутримышечного укола).
При пероральном приеме лекарственых средств не нужны какие-то дополнительные гаджеты и медицинский персонал рядом, что значительно упрощает прием. Однако лекарство, принятое внутрь через рот, очень медленно воздействует на цель, поскольку прежде, чем поступить в кровь, оно должно дойти, раствориться и расщепиться в желудочно-кишечном тракте, параллельно довольно сильно его раздражая и вызывая проблемы в его функционировании и даже сложные заболевания. К тому же, печеночные ферменты, призванные выводить остатки лекарства, способны начать его выведение еще до полного воздействия, что часто снижает эффективность влияния лекарства (его биодоступность) и заставляет продлевать терапевтические курсы.
Всего этого можно избегать, применяя инъекционную методику введения лекарств, однако уколы – процедура болезненная. К тому же высокий риск развития тромбоэмболии при попадании воздуха в сосуды во время инъекции или флебитов (воспалительный процесс, венозных стенок).
При введении лекарств с помощью электрофореза пациент не будет ощущать никакого дискомфорта, у него не возникнут аллергические и иные реакции общего или местного характера, а терапевтический эффект от вводимого препарата может длиться от суток до 20 дней. К тому же, существует возможность введения средства для лечения непосредственно в воспаленное место, минуя желудочно-кишечный тракт и сосудистую систему организма.
Недостатков у данного метода немного – это факт того, что не каждое лекарство можно вводить с помощью электрофореза, и, конечно же, индивидуальные противопоказания для его проведения у пациента.
Техника и методы проведения процедуры
Перед началом процедуры кожа пациента должна быть очищена. При наличии повреждений кожных покровов данные участки необходимо обработать вазелином, и покрыть ватой, резиной или клеенкой.
Электроды накладываются продольно (воздействие на поверхностные ткани) и поперечно (влияние на глубокие тканы и органы). Возможно расположение поперечно-диагонально.
При проведении процедуры больной занимает сидячее или лежачее положение. Электроды крепятся при помощи лейкопластыря, бинта, или небольших емкостей с песком.
Существуют различные методы применения гальванизации:
- Общая. Применяется гидрогальваническая ванна, состоящая из четырех отдельных ванн с водой, в которые погружаются конечности пациента. Сила тока не превышает 30 мА.
- Местная. Применяются 2-4 свинцовых электрода, которые накладываются на тело больного.
-
Обработка
рефлекторно-сегментарных зон. Воздействие на паравертебральные участки позвоночника. Применяются электроды для воротниковой зоны и электрод «трусы». Сила тока начинается с 6 мА и наращивается постепенно до 16 мА (в течение нескольких сеансов). - Продольная гальванизация головы. Используется два электрода: один на лбу, другой в области затылка и шеи.
- Метод Бургиньона. На сомкнутые веки пациента помещают кусочки марли, покрывают сверху круглыми металлическими пластинками, которые соединены с зажимом аппарата гальванизации. Второй электрод расположен под затылочным бугром. Волосы пациента обильно увлажнены.
- Гальванизация области лица. На лицо пациента помещают электрод-«полумаску». Прилегание должно происходить в области подбородка, щеки и лба. Угол рта и глаз остаются свободными.
- Применение процедуры при поражениях нервов верхних и нижних конечностей. При поражении верхних конечностей электроды накладывают на нижние шейные и верхние грудные позвонки, область предплечья. При терапии нижних конечностей область наложения электродов зависит от места поражения.
- Камерные ванны. В зависимости от необходимого количества точек воздействия (количество конечностей) применяют одно-, двух-, трех- и четырехкамерные ванны.
Типы мембран
Самая важная часть ионоселективного электрода, ионоселективная мембрана, имеет состав, который варьируется в зависимости от определяемого иона. Наиболее важными типами мембран являются кристаллические или стекловидные твердые тела или композиты с полимерами.
Стеклянные мембраны
Стеклянные мембраны обычно обладают отличной химической стойкостью и в основном используются для pH-электродов и электродов для отбора натрия.
Кристаллические мембраны
Кристаллические мембраны могут быть поликристаллическими или монокристаллическими. Монокристаллические мембраны из фторида лантана используются для большинства фторидных электродов .
Мембраны на полимерной основе
Мембраны на основе полимеров могут состоять из ионообменной смолы . Одним из примеров является калий-селективный электрод, который содержит валиномицин в качестве переносчика ионов ( ионофор ).
9.5 Определение электрического сопротивления ионоселективных электродов
Примечание — Определение электрического сопротивления проводят в конце поверки.
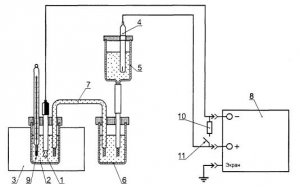
9.5.1 Для определения электрического сопротивления используют установку, изображенную на рисунке А.1 приложения А.
9.5.2 Термостатируют в течение 30 мин ячейку 2 при температуре, указанной в ЭД.
9.5.3 Измеряют потенциал Е1ионоселективного электрода относительно электрода сравнения в контрольном растворе с концентрацией, указанной в ЭД.
9.5.4 С помощью переключателя 11 подключают (на время не более 5 с) между поверяемым электродом и электродом сравнения калиброванное сопротивление Rk 10, равное (10,0±0,5) МОм — для ионоселективных электродов с R ? 10 МОм или (620±30) кОм — для ионоселективных электродов R < 10 МОм.
9.5.5 Измеряют потенциал Е2 ионоселективного электрода с подключенным калиброванным сопротивлением.
9.5.6 Рассчитывают электрическое сопротивление ионоселективного электрода R, МОм, по формуле
R = Rk(Е1/E2 — 1). (3)
9.5.7 Результаты поверки считают положительными, если сопротивление электрода соответствует значению, указанному в ЭД.
10 Оформление результатов поверки
10.1 Результаты поверки должны быть оформлены в виде протокола.
10.2 Если электрод по результатам поверки признан пригодным к применению, то на него выдают «Свидетельство о поверке» в соответствии с ПР 50.2.006 или наносят поверительное клеймо в соответствии с ПР 50.2.007 .
10.3 При отрицательных результатах поверки выдают «Извещение о непригодности» по ПР 50.2.006 с указанием причин, а электрод к применению не допускают.
ПРИЛОЖЕНИЕ А
(обязательное)
Установки для поверки ионоселективных электродов
 Р 50.2.034-2004 ГСИ. Электроды ионоселективные для определения активности ионов в водных растворах. Методика поверки
Р 50.2.034-2004 ГСИ. Электроды ионоселективные для определения активности ионов в водных растворах. Методика поверки
1 — поверяемый электрод; 2 — термостатируемая ячейка с контрольным раствором; 3 — термостат; 4 — электрод сравнения хлорсеребряный насыщенный эталонный 2-го разряда; 5 — сосуд для электрода сравнения; 6 — сосуд с насыщенным раствором хлорида калия; 7 — электролитический ключ; 8 — иономер-милливольтметр; 9 — термометры; 10 — калиброванное сопротивление; 11 — переключатель
Рисунок А.1 — Схема установки для поверки ионоселективных электродов (кроме комбинированных)
 Р 50.2.034-2004 ГСИ. Электроды ионоселективные для определения активности ионов в водных растворах. Методика поверки
Р 50.2.034-2004 ГСИ. Электроды ионоселективные для определения активности ионов в водных растворах. Методика поверки
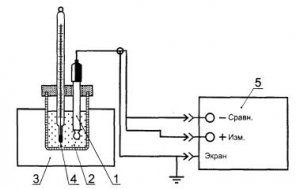
1 — поверяемый электрод; 2 — термостатируемая ячейка с контрольным раствором; 3 — термостат; 4 — термометр; 5 — рН-метр-милливольтметр
Рисунок А.2 — Схема установки для поверки комбинированных ионоселективных электродов
ПРИЛОЖЕНИЕ Б
(справочное)
Библиография
ПР 50.2.006-94 Государственная система обеспечения единства измерений. Порядок проведения поверки средств измерений
ПР 50.2.007-94 Государственная система обеспечения единства измерений. Поверительные клейма
История развития ионоселективных электродов:
Как ни странно, но история развития ионоселективных мембранных
электродов связана с физиологическими исследованиями. В середине ХIХ века
физиологи обнаружили, что между отдельными частицами организмов возникает
разность электрических потенциалов. Для понимания процессов, протекающих в
сложных биологических мембранах, в конце ХIХ химиками были созданы простейшие прототипы
мембран.
В 1890 году воспользовавшись понятием полупроницаемой
мембраны, Вильгельм Фридрих Оствальд создал модель биологической мембраны и
доказал, что предельное значение разности потенциалов в такой мембране достигается
только в случае жидкостного потенциала, при условии, что один из ионов
статичен, и его подвижность равна нулю.
Настоящим прорывом в ионометрии стало открытие в начале ХХ столетия
способности реагирования стеклянной мембраны на изменение концентрации ионов
водорода. Первые основные исследования потенциалов стеклянных мембран были
проведены М. Кремером и Ф. Габером. Они же создали и испытали первые прототипы
стеклянных электродов с жидкими и твердыми мембранами.
Первые стеклянные электроды, которые можно было применять на
практике для измерения уровня pH
в электролитических растворах, были предложены Юзом, Никольским и Шульцем,
Долом и Мак-Иннесом в 20-х годах. В 50-х годах были созданы стеклянные
электроды на базе ионов щелочных металлов, из которых наибольшее практическое
значение имел натриевый стеклянный электрод.
Электроды с жидкими мембранами, которые содержали
растворенный ионит, впервые подверглись изучению Соллнером и Шином. Однако,
такие мембраны не обладали достаточной селективностью, относительно какого-либо
определенного иона.
Первым прототипом современных ионоселективных электродов можно
считать сенсор Кларка. Он был создан в 60-х годах XX века и использовался для
определения концентрации кислорода в растворах.
Существует множество классификаций ионоселективных
электродов, однако, наиболее правильным в настоящее время будет выделение вида
электрода в зависимости от типа мембраны и в зависимости от функциональных
особенностей.
Исторический
Основная структура ионоселективных электродов и концентрационная зависимость напряжения были известны уже в первой половине 20 века: Зигмунт Клеменсевич открыл принцип действия pH-электрода в лаборатории Фрица Габера, а Изаак Колтофф исследовал клетки с мембранами из галогенида серебра. Практическое применение стеклянного электрода пришло после того, как были использованы улучшенные формы и стекла, а также после того, как Арнольд Орвилл Бекман разработал чувствительное устройство для измерения напряжения. Целенаправленная разработка и применение других ионоселективных электродов не происходило до 1950-х и 1960-х годов, например Б. 1957 г. анонсирован натриевый электрод. В 1962 году производитель стекла Corning основал компанию Orion Research для разработки новых электродов. В 1966 году он представил кальциевый и фторидный электроды, а в 1967 году в его ассортименте было девять различных электродов (для Ag +, Ca 2+, Cu 2+, F -, Br -, I -, ClO 4 -, NO 3 — и S 2. — ).
Перекрестная чувствительность
Идеальный ионоселективный электрод будет специфичным для ионов; то есть он будет реагировать только на определяемый ион и не будет реагировать на другие ионы. На практике ионоселективные электроды часто перекрестно чувствительны к другим ионам; поэтому IUPAC рекомендует не использовать термин «ионно-специфический». Например, многие электроды pH реагируют не только на протоны, но и на высокие концентрации ионов натрия, особенно при высоких значениях pH. Фторидные электроды чувствительны к гидроксид-ионам. Поэтому ионоселективный электрод редко бывает полностью ион-специфичным, и поэтому для точного анализа необходимо учитывать возможное перекрестное влияние других ионов. Количественное описание можно сделать с помощью уравнения Никольского-Эйзенмана:
- Э.знак равноЭ.∘+Р.ТzА.Ф.пераА.+∑Б.(KА.,Б.пОт аБ.zА.zБ.){\ displaystyle E = E ^ {\ circ} + {\ frac {RT} {z _ {\ mathrm {A}} F}} \ ln };
Примеры коэффициентов селективности можно найти в.
KА.,Б.пОт{\ Displaystyle К _ {\ mathrm {A, B}} ^ {\ mathrm {горшок}}}
Электрофорез, как улучшенный метод гальванизации
Сочетание гальванизации с лекарственными средствами называется электрофорезом. Гальванический ток применяется для более результативного усвоения лекарственных препаратов организмом, и делает их воздействие эффективным и мягким.
Лекарственные растворы вводятся в организм через слизистые оболочки и кожные покровы под воздействием электрического поля. Наиболее эффективным является воздействие на волосяные фолликулы, протоки сальных желез, межклеточные промежутки и потовые железы.
В лекарственных препаратах, применяемых при электрофорезе, содержатся ионы (заряженные частицы), которые вводятся в организм различными электродами. Выбор электрода зависит от заряда ионов. Во время одной процедуры с разных точек воздействия могут вводиться различные вещества.
Процедура электрофореза является безболезненной, однако возможны дискомфортные ощущения в виде легкого покалывания в области наложения электродов.
Электрофорез рекомендован при таких неврологических заболеваниях:
- неврозы;
- воспалительные процессы;
- мигрень;
- органические заболевания центральной нервной системы;
- неврастения.
Электрофорез может проводиться различными путями:
- Через кожные покровы – электроды размещаются на коже пациента.
- При помощи ванночек – в резервуар с встроенными электродами помещается раствор лекарственного вещества, и в данную «ванночку» помещается часть тела, требующая воздействия.
- Полостным методом – раствор лекарственного препарата вводится ректально или во влагалище. Электрод также вводится внутрь. С наружной части тела крепится электрод, имеющий другую полярность (применяется для терапии болезней толстого кишечника и органов малого таза).
- Внутритканевым методом – препарат вводится перорально, ингаляционно, внутривенно, электроды накладываются на пораженный орган или область (наиболее эффективно при болезнях органов дыхания).
В результате процедуры лекарственные вещества накапливаются в кожных покровах, и могут оставаться там от 12 часов до 20 суток. За счет этого обеспечивается более длительное воздействие препаратов, и медленное выведение их из организма.
Преимущество метода в том, что накопление лекарственного препарата происходит локально, не распространяя его на весь организм.
Концентрация лекарства в области применения в несколько раз превышает концентрацию при обычных способах ввода. Электрофорез позволяет ввести лекарства в области с нарушением микроциркуляции и кровообращения, куда обычно проникновение медпрепаратов затрудняется. Положительной чертой метода также является низкий уровень аллергических и побочных реакций.
9.3 Определение крутизны градуировочной характеристики электрода
9.3.1 Для определения крутизны градуировочной характеристики ионоселективных электродов используют установку, указанную в 9.2.1.
9.3.2 Термостатируют в течение 30 мин ячейку 2 при температуре, указанной в НД.
9.3.3 Проводят измерение потенциалов электрода не менее двух раз в каждом из трех контрольных растворах с концентрацией ионов, соответствующей началу, середине и концу линейного участка градуировочной характеристики.
Примечание — Определение потенциала начинают с контрольного раствора с наименьшей концентрацией, затем переходят к более концентрированным растворам. Перед проведением измерений электрод промывают тем раствором, в котором будут проводить определение.
9.3.4 Определяют градуировочную характеристику Е(рХ) путем расчета по измеренным точкам регрессионной линии по методу наименьших квадратов.
Примечание — Значения рХ для контрольных растворов различной концентрации должны быть приведены в ЭД на данный ионоселективный электрод. При добавлении в контрольные растворы БРОИС, в соответствии с ЭД на ионоселективный электрод, в расчетах необходимо использовать значение рХ = — lg Cx.
9.3.5 Рассчитывают значение крутизны градуировочной характеристики S, мВ/рХ, по формуле
(1)
где Е1, Е2— значения потенциалов электрода на градуировочной характеристике, мВ, соответствующие рХ1, рХ2.
9.3.6 Результаты поверки считают положительными, если расчетное значение крутизны электродной характеристики электрода не менее приведенного в ЭД.
Место в неврологической и общемедицинской практике
Гальванизация является эффективным методом терапии таких неврологических заболеваний:
- поражение периферической и центральной нервных систем в результате травматического, токсического и инфекционного воздействия;
- неврозы;
- последствия травм спинного и головного мозга;
- неврит;
- нарушение кровообращения в спинном и головном мозге;
- рассеянный склероз;
- параличи, парезы;
- энцефалопатия;
- остеохондроз.
Также гальванизация широко применяется в таких областях медицины:
- кардиология;
- гастроэнтерология;
- урология;
- пульмонология;
- стоматология;
- ЛОР;
- хирургия;
- эндокринология;
- ортопедия;
- гинекология;
- косметология;
- дерматология;
- офтальмология.
Исторические аспекты методики
Впервые об электрофорезе было заявлено немецким ученым Фердинандом Рейсом, который в 1809 году плотно изучал эту методику, однако развития в тот период данное направление не получило. Лишь в 1926 году шведским биохимиком Арне Тиселиусом была опубликована научная работа с описанием специальной трубки для проведения электрофореза, которую к 1930 году усовершенствовали, начав изготавливать ее из хлорида серебра.
Лишь в 1936 году был опробован первый аппарат, предназначенный для проведения электрофореза. При этом форма трубок снова претерпела многократные изменения, сначала превратившись в узкие ячейки, а затем – в стеклянные секции. Такие перемены повышали оптическую восприимчивость прибора и позволяли ему активнее удалять тепло, выделяемое в ходе прохождения электротока. Тестирование аппарата впервые выполнено на лошадиной сыворотке. В процессе электрофореза препарат разделялся на полоски белого цвета, что свидетельствовало о разной скорости миграции белков крови, альфа, бета и гамма-глобулина, а также альбумина. После такого успеха тесты провели на кроличьей, а затем и на человеческой сыворотке и результаты получены были аналогичные.
Таким образом было установлено, что молекулы с электрическими зарядами в жидкой среде могут под действием электромагнитных полей перемещаться в противоположную заряженным электродам область. При использовании параллельно с электрофорезом ультрацентрифуги в последующих опытах Тиселиус смог точнее дифференцировать направление миграционных процессов белков и установил количество протеинов в составе.
Уже в 1950 году был проведен новый, более усовершенствованный опыт по разделению белков на поверхности фильтровальной бумаги, которая затем резалась на полоски, окрашивалась для определения содержания отдельных белков в подобных растворах. При этом удалось зафиксировать процесс миграции белков и получить четкие границы их разделения. Метод электрофореза на различных носителях в настоящее время широко используется в биохимии, молекулярной биологии, генной инженерии, а также медицине.
Сегодня с помощью электрофореза врачи диагностируют:
- инфекционно-воспалительные процессы;
- заболевания печени и почек;
- иммунные и генетические нарушения;
- онкологические новообразования.
Также современная медицина использует электрофорез с белковыми и коллоидными растворами для физиотерапевтических методик при лечении многих заболеваний.
Классификация
Классификация электродов электрохимические. 1-го рода — металлические или газовые, погруженные в раствор электролита, содержащего ионы материала. Такие оборотные до сих ионов. Напр. на серебряном Е.Е. Ag | Ag + происходит потенциалотвирна реакция: AgDAg + + 1ē.
В газовых электродах электрохимических роль металла должны играть электрохимические активные газы (водород, хлор, кислород и др.), но они не являются электронными проводниками тока, поэтому электрический контакт в газовых электрохимических электродах осуществляется с помощью инертных металлов (платины, золота, палладия), которые служат передатчиками электронов от молекул газов к ионам раствора и наоборот. Например, хлорный электрод Pt, Cl2 | Cl- представляет собой платиновую пластинку, которая погружена в раствор с Сl — ионами и омывается равномерным потоком газа Cl2 с давлением РCl2. Газ Cl2 адсорбируется на платиновой пластинке, затем распадается на атомы Clадс, которые уже принимают непосредственное участие в электрохимической реакции: Cl2 2arrow.eps 2Clадс 2arrow.eps 2Cl- + 2ē.
К электродам 1-го рода относятся также амальгамные, например, натриевый амальгамный, в котором роль металлического ингредиента играет амальгама натрия. На таком Е.Е. потенциалотвирна реакция проходит следующим образом: Na + + ē (Hg) 2arrow.eps Na (Hg).
Электроды электрохимические 2-го рода — это металлы, покрытые слоем своей труднорастворимые соли и погружены в раствор электролита, содержащий общий анион из труднорастворимых солью. К этой группе относятся электроды сравнения — хлорсеребряный (Ag, AgCl | Cl-), каломельный (Hg, Hg2Cl2 | Cl-), сульфатртутний (Hg, HgSO4 | SO42-). Потенциалообразущая реакция, например. на хлорсеребряный Е.Е., проходит следующим образом: AgCl + ē 2arrow.eps Ag + Cl-.
Электрохимические электроды 3-го рода — это металлы, покрытые двумя слоями двух труднорастворимых солей. Первая соль меньше растворимый, чем вторая, и содержит катион металла электрохимический электрод. Вторая соль больше растворимый, чем первая, удерживает тот же анион, что и первая. Например, оксалатный электрод 3-го рода Ag, Ag2C2О4, CaC2O4 | Ca2 +.
Потенциалотвирна реакция на таком Электрохимические электроды проходит следующим образом: Ag2C2О4 + 2ē + Са 2+ 2arrow.eps 2Ag + CаС2О4.
Окислительно-восстановительные электрохимические электроды (Редокс-электроды) — это металлы, материал которых не участвует в электрохимической реакции, а лишь выполняет роль передатчика электронов от восстановленной формы к окисленной или наоборот. Напр .: Fe3 + + 1ē 2arrow.eps Fe2 +. В такой реакции окислительно-восстановительный Е.Е. осуществляет перенос электронов между этими ионами.
где аокис., авидн. — активность окисленной и восстановленной форм соответственно; n — количество электронов, которая участвует в окислительно-восстановительной реакции.
Модифицированные электрохимические электроды, поверхность которых модифицируют с помощью физических или химических методов с целью придания ей определенных характеристик. Например, при физической модификации проводят ионную имплантацию, разрыхление поверхности или выращивания на ней монокристаллических структур и тому подобное. При химической модификации поверхности электрода покрывают органическими, металлоорганическими или неорганическими слоями, создают на поверхности. Композиты с электродных материалов, изменяют химический состав поверхности устройства тому подобное. В частности, химической модификацией поверхности ионоселективных видов с функциями неорганических ионов были получены ионселективные электроды с функциями органических ионов лекарственных веществ: прокаина, лидокаина, диклофенака натрия и др.
Конструкции и размер электрохимические электроды разнообразны. Они бывают в виде стержня, пластинки, шарики, сетки и т.п. Поверхность ультрамикроелектродив не превышает 10-14 м2. Е.Е., которые используют в электроаналитические методах анализа, имеют поверхность около 10-5 м2; электроды, которые используют в электрохимическом синтезе лекарственных веществ, например, глюконата кальция, имеют поверхность более 10-2 м2.
см. также Ионоселективные электроды.
Важные ионы, которые можно определить с помощью ионоселективных электродов
Предстоит определить ионоселективные электроды для более чем 50 ионов. Коммерчески доступные, которые доступны для следующих ионов, особенно важны для практического применения:
Катионы
- одновалентные катионы M 1+ : протоны H + или pH, натрий Na +, калий K +, серебро Ag +, аммоний NH 4 +
- двухвалентные катионы M 2+ : медь Cu 2+, свинец Pb 2+, кальций Ca 2+, кадмий Cd 2+, барий Ba 2+
Анионы
- Галогениды : фторид F -, хлорид Cl -, бромид Br -, йодид I — ,
- Прочие: сульфид HS — / S 2-, цианид CN -, нитрат NO 3 -, перхлорат ClO 4 -, фторборат BF 4 -, тиоцианат SCN —
Клинически важными ионами, которые определяются с помощью ионоселективных электродов, являются H +, Na +, K +, Ca 2+ и Cl — .
Основные параметры процедуры
Процедура гальванизации в физиотерапии может проводиться с различной дозировкой плотности, силы тока и по длительности воздействия. Для данного физиотерапевтического метода применяют ток невысокого напряжения (до 80 В) и незначительной силы (до 50 мА). Плотность тока варьируется от 0,01 мА/см2 до 0, 08 мА/см2.
Наиболее сильный ток применяют при терапевтическом воздействии на туловище и конечности (от 15 мА до 30 мА). При наложении электродов на область головы, лица, слизистых оболочек сила тока не превышает 5 мА.
Ток к телу пациента подводится при помощи электродов (свинцовые пластины толщиной до 1 мм, с влажной прокладкой, и подведенный к пластине шнур). Также электроды могут быть встроены в резервуар («ванночку»), применяемый для погружения в него части тела, требующей терапии. Гидрофильная прокладка и вода в резервуаре необходимы для предупреждения ожога кожных покровов пациента продуктами электролиза.
Электроды могут иметь прямоугольную форму, быть в виде полумаски (применение на лице), в виде «воротника» (для воздействия на верхнюю часть спины и надплечий), в виде воронки (для применения в области ушей), «ванночка». Также существуют полостные электроды для внутривлагалищного и ректального применения.
После закрепления электродов на теле пациента, или помещения части тела в «ванночку» запускается ток, и постепенно наращивается до достижения необходимых параметров. Процедура завершается постепенным уменьшением тока до его выключения.
Электроды могут быть наложены поперечно или продольно. Поперечное наложение способствует более эффективному воздействию на глубокорасположенные ткани. Электроды располагаются на противоположных участках тела, напротив друг друга. Продольное расположение обеспечивает воздействие на поверхностные участки тканей. Электроды накладываются на одну сторону тела.
После проведения 5-7 сеансов гальванизации состояние пациента может ухудшиться. Данный эффект обозначает положительный эффект от проведенных процедур.
Длительность процедуры составляет от 15 минут (при общем воздействии) до 40 минут (при местном воздействии). Терапевтический курс состоит из 10-20 сеансов гальванизации. Рекомендовано проведение процедуры ежедневно или через день. Прохождение повторного курса возможно через месяц.
Описание
Ионометрия на данный момент является достаточно широкой областью знаний, занимающей отдельную нишу в современной аналитической химии.
Как и в любом другом научном направлении, тут так же необходимо в ряде случаев привлекать различные методы исследования для решения тех или иных проблем. К одной из них относится необходимость определения содержания ионов в различных электролитических растворах.
Ионоселективные электроды – устройства, потенциал которых в электролите определяется содержанием ионов. Это позволяет использовать их для установления содержания ионов, а также контролировать и отслеживать его изменение во время различных процессов.
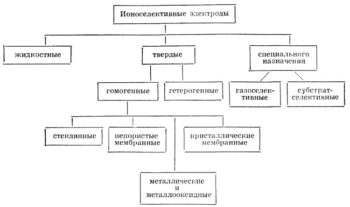 Виды ионоселективных электродов.
Виды ионоселективных электродов.
Если какая-либо реакция приводит к изменению исходного состава, то данные приборы позволят проанализировать такие процессы и детально их изучить.
Селективный электрод обладает рядом преимуществ, среди них:
- отсутствие воздействия на исследуемый раствор;
- портативность.
На данный момент существует большое количество классификаций подобных приборов. Однако наиболее правильным является разделение по типу используемой мембраны, а также особенностям применения устройства.
Особенности использования
Ионоселективные электроды являются неотъемлемыми приборами в решении многих научных и технических задачах. В зависимости от ситуации выбирается определенный тип устройства.
По функциональности их разделяют на измерительные, вспомогательные, комбинированные. В первом случае они способны работать, как индикаторы и измерители.
Вспомогательные работают в паре с измерительными, и служат для сравнения показаний со стандартным раствором. Комбинированный тип сочетает в себе функциональность приведенных выше вариантов.
По типу мембраны выделяют несколько вариантов устройств. Это могут быть твердые, жидкостные, газовые и энзимные электроды.
В первом случае используются кристаллы солей труднорастворимых в воде. Основой жидких мембран являются растворы ионообменных веществ. Это могут быть жидкие катионы и анионы, а также хелатные соединения.
Газовый включает в себя два электрода. Один из них – ионоселективный, а второй – вспомогательный. Они контактируют со вспомогательным раствором, отделенного прослойкой из газа или же гидрофобной мембраной. К преимуществам данных устройств можно отнести длительный срок службы.
История данных электродов берет свое начало, как это ни удивительно, с физиологических исследований. Еще в середине девятнадцатого века ученые обнаружили, что между различными частичками организмов появляется электрохимический потенциал.
Уже в конце девятнадцатого века были созданы первые простейшие мембраны, позволяющие понять процессы, происходящие в сложных мембранах.
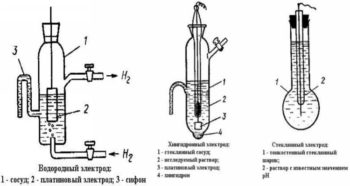 Разновидности электродов для измерения РН.
Разновидности электродов для измерения РН.
В пятидесятых года прошлого века были изготовлены и первые стеклянные электроды. Они позволяли определять содержание ионов H2.
Практическое использование данных приборов стало возможным только в двадцатых годах прошлого столетия. Позже были изготовлены устройства, в основе принципа работы которых лежали щелочные металлы.
Данные устройства портативны и просты в использовании. Кроме того, подобные приспособления не оказывают никакого воздействия на исследуемые объекты. Благодаря таким существенным преимуществам их широко применяют в различных научных целях.
На данный момент существует большое множество подобных приспособлений, так что их можно выбрать для любых целей.
При выборе электрода не стоит забывать о том, что в зависимости от назначения и области использования они могут подключаться к различным устройствам.
Если речь идет о приспособлениях общего назначения, то их можно подключать к разным приборам. А вот устройства специального назначения могут работать только с конкретными аппаратами и использоваться только в определенных условиях.






























