Сплав Вуда
В 1860 г. американский зубной техник Барнабас Вуд искал оптимальные соотношения компонентов, чтобы изготавливать зубы для клиентов при минимальных температурах плавления. Им был найден сплав, который имеет температуру плавления всего 60,2…68,5 ⁰С. Даже в горячей воде металл легко расплавляется. В него входят:
- олово — 12,5…12,7 %;
- свинец — 24,5…25,0 %;
- висмут — 49,5…50,3 %;
- кадмий — 12,5…12,7 %.
Сплав интересен своей низкой температурой, но практического применения так и не нашел
Внимание! Кадмий и свинец – это тяжелые металлы, контакт с ними не рекомендован. У многих людей могут происходить отравления при контакте с кадмием
Месторождения и запасы
Залежи различных руд, из которых добывают ценные и простые металлы, разбросаны по всему миру. Запасы металлических примесей, по оценкам экспертов в мировом масштабе, составляют более восьмидесяти миллиардов тонн. Основные залежи расположены на территории таких стран как:
- Россия;
- Бразилия;
- Австралия.
Самые богатые из месторождений, известных добычей железных руд – это Горно-обогатительные комбинаты, расположенные на территории Курской магнитной аномалии, которую считают самым крупным мировым источником ресурса. Кроме этого известны такие месторождения, как Белорецкое, Оленегорское, Костомукшское, Качканарское и Магнитогорское.
Характерным отличием железных руд, обнаруженных в последнем из перечисленных месторождений, является избыток серы в составе руды, чего нет у ископаемых, которые добывают в других местах. Именно этим она и представляет ценность.
В развитых странах, геологи занимаются поиском и находят рудные породы, а промышленники выполняют добычу и переработку руд в необходимое сырье. Некоторые слаборазвитые страны, которые располагают большими залежами железной руды, занимаются добычей и экспортом сырья. Например, Венесуэла добывает 20 млн. т полезных руд, большую часть которых, отправляет в США.
В последние годы изделия из металла стараются заменить новыми современными полимерными материалами. Однако это не уменьшает спрос на металлическое сырье, а лишь конкретизирует сферы, которые не могут обойтись без заготовок, изготовленных из железных руд.
Рейтинг: /5 —
голосов
Свойства [ править ]
Физический
Свойства тугоплавких металлов
| Имя | Ниобий | Молибден | Тантал | Вольфрам | Рений |
| Период | 5 | 5 | 6 | 6 | 6 |
| Точка плавления K | 2750 | 2896 | 3290 | 3695 | 3459 |
| Точка кипения K | 5017 | 4912 | 5731 | 6203 | 5869 |
| Температура плавления, ° C | 2477 | 2623 | 3017 | 3422 | 3186 |
| Температура кипения, ° C | 4744 | 4639 | 5458 | 5930 | 5596 |
| Плотность г · см –3 | 8,57 | 10,28 | 16,69 | 19,25 | 21.02 |
| Модуль Юнга ГПа | 105 | 329 | 186 | 411 | 463 |
| Твердость по Виккерсу МПа | 1320 | 1530 | 873 | 3430 | 2450 |
- ^ ab Согласованные значения взяты из точек плавления элементов с множественными ссылками.
- ^ ab Согласованные значения взяты из точек кипения элементов с множественными ссылками. Вольфрам имеет особенно широкую полосу расхождений: два основных источника показывают 5555 ° C.
- Согласованные значения взяты из плотностей элементов с множественными ссылками.
Тугоплавкие металлы имеют высокие температуры плавления, вольфрам и рений — самые высокие из всех элементов, а температуры плавления других металлов превышают только осмий и иридий , а также сублимацию углерода . Эти высокие температуры плавления определяют большинство их применений. Все металлы являются объемно-центрированными кубическими, за исключением рения, который имеет гексагональную плотную упаковку . Большинство физических свойств элементов этой группы значительно различаются, потому что они принадлежат к разным группам .
Сопротивление ползучести — ключевое свойство тугоплавких металлов. В металлах начало ползучести коррелирует с температурой плавления материала; ползучесть в алюминиевых сплавах начинается при 200 ° C, тогда как для тугоплавких металлов необходимы температуры выше 1500 ° C. Это сопротивление деформации при высоких температурах делает тугоплавкие металлы пригодными для противодействия сильным воздействиям при высокой температуре, например, в реактивных двигателях или инструментах, используемых во время ковки .
Химическая
Тугоплавкие металлы демонстрируют широкий спектр химических свойств, потому что они входят в три отдельные группы периодической таблицы . Они легко окисляются, но в массивном металле эта реакция замедляется за счет образования устойчивых оксидных слоев на поверхности. В частности, оксид рения более летуч, чем металл, и поэтому при высокой температуре теряется стабилизация против воздействия кислорода, поскольку оксидный слой испаряется. Все они относительно устойчивы к кислотам.
Кристаллические решетки
Кристаллической решеткой называют пространственное расположение атомов или ионов в кристалле. Точки кристаллической решетки, в которых расположены атомы или ионы, называют узлами кристаллической решетки.
Кристаллические решетки подразделяют на молекулярные, атомные, ионные и металлические.

Очень важно не перепутать вид химической связи и кристаллической решетки. Помните, что кристаллические решетки отражают пространственное расположение атомов
Молекулярная кристаллическая решетка
В узлах молекулярной решетки расположены молекулы. При обычных условиях молекулярную решетку имеют большинство газов и жидкостей. Связи чаще всего ковалентные полярные или неполярные.
Классическим примером вещества с молекулярной решеткой является вода, так что ассоциируйте свойства этих веществ с водой. Вещества с молекулярной решеткой непрочные, имеют небольшую твердость, летучие, легкоплавкие, способны к возгонке, для них характерны небольшие температуры кипения.
Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2. Особо хочется отметить красный и белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы подробно изучили в статье, посвященной классификации веществ.

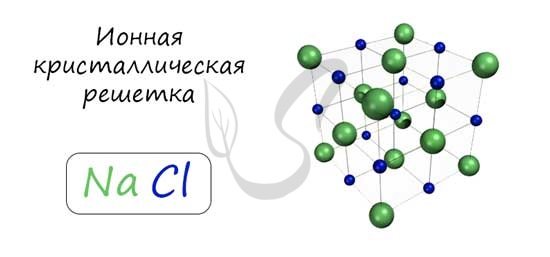
Ионная кристаллическая решетка
В узлах ионной решетки находятся атомы, связанные ионной связью. Этот тип решетки характерен для веществ, обладающих ионной связь: соли, оксиды и гидроксиды металлов.
Ассоциируйте этот ряд веществ с поваренной солью — NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.
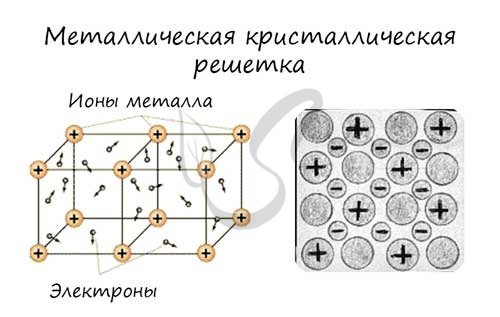
Металлическая кристаллическая решетка
В узлах металлической решетки находятся атомы металла. Этот тип решетки характерен для веществ, образованных металлической связью.
Ассоциируйте свойства этих веществ с медью. Они обладают характерным металлическим блеском, ковкие и пластичные, хорошо проводят электрический ток и тепло, имеют высокие температуры плавления и кипения.
Примеры: Cu, Fe, Zn, Al, Cr, Mn.
Атомная кристаллическая решетка
В узлах атомной решетки находятся атомы, связанные ковалентной полярной или неполярной связью.
Ассоциируйте эти вещества с песком. Они очень твердые, очень тугоплавкие (высокая температура плавления), нелетучие, прочные, нерастворимы в воде.
Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), черный фосфор (P).

Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию
Физические свойства
Железо — типичный металл, в свободном состоянии — серебристо-белого цвета с сероватым оттенком. Чистый металл пластичен, различные примеси (в частности — углерод) повышают его твёрдость и хрупкость. Обладает ярко выраженными магнитными свойствами. Часто выделяют так называемую «триаду железа» — группу трёх металлов (железо Fe, кобальт Co, никель Ni), обладающих схожими физическими свойствами, атомными радиусами и значениями электроотрицательности.
Для железа характерен полиморфизм, оно имеет четыре кристаллические модификации:
- до 769 °C существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика (769 °C ≈ 1043 K — точка Кюри для железа);
- в температурном интервале 769—917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмно-центрированной кубической решётки и магнитными свойствами парамагнетика;
- в температурном интервале 917—1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой;
- выше 1394 °C устойчиво δ-Fe с объёмно-центрированной кубической решёткой.
Металловедение не выделяет β-Fe как отдельную фазу, и рассматривает её как разновидность α-Fe. При нагреве железа или стали выше точки Кюри (769 °C ≈ 1043 K) тепловое движение ионов расстраивает ориентацию спиновых магнитных моментов электронов, ферромагнетик становится парамагнетиком — происходит фазовый переход второго рода, но фазового перехода первого рода с изменением основных физических параметров кристаллов не происходит.
Для чистого железа при нормальном давлении, с точки зрения металловедения, существуют следующие устойчивые модификации:
- от абсолютного нуля до 910 °C устойчива α-модификация с объёмноцентрированной кубической (ОЦК) кристаллической решёткой;
- от 910 до 1400 °C устойчива γ-модификация с гранецентрированной кубической (ГЦК) кристаллической решёткой;
- от 1400 до 1539 °C устойчива δ-модификация с объёмно-центрированной кубической (ОЦК) кристаллической решёткой.
Наличие в стали углерода и легирующих элементов существенным образом изменяет температуры фазовых переходов (см. фазовую диаграмму железо—углерод). Твёрдый раствор углерода в α- и δ-железе называется ферритом. Иногда различают высокотемпературный δ-феррит и низкотемпературный α-феррит (или просто феррит), хотя их атомные структуры одинаковы. Твёрдый раствор углерода в γ-железе называется аустенитом.
В области высоких давлений (свыше 13 ГПа, 128,3 тыс. атм.) возникает модификация ε-железа с гексагональной плотноупакованной (ГПУ) решёткой.
Явление полиморфизма чрезвычайно важно для металлургии стали. Именно благодаря α—γ переходам кристаллической решётки происходит термообработка стали
Без этого явления железо как основа стали не получило бы такого широкого применения.
Железо относится к умеренно тугоплавким металлам. В ряду стандартных электродных потенциалов железо стоит до водорода и легко реагирует с разбавленными кислотами. Таким образом, железо относится к металлам средней активности.
Температура плавления железа 1539 °C, температура кипения — 2862 °C.
Температура плавления металлов
Разные вещества имеют различную температуру плавления. Принято делить металлы на:
- Легкоплавкие – их достаточно нагревать до 600 ⁰С, чтобы получать вещество в жидком виде.
- Среднеплавкие металлы расплавляются в диапазоне температур 600…1600 ⁰С.
- Тугоплавкими называют металлы, которые могут расплавляться при температуре более 1600 ⁰С.
В таблице по возрастанию показаны легкоплавкие металлы. Здесь видно, что самым необычным металлом является ртуть (Hg). В обычных условиях она находится в жидком состоянии. Этот металл имеет самую низкую температуру плавления.
Таблица 1, температуры плавления и кипения легкоплавких металлов:
Таблица 2, температуры плавления и кипения среднеплавких металлов:
Таблица 3, температуры плавления и кипения тугоплавких металлов:
Чтобы вести процесс плавки используют разные устройства. Например, для выплавки чугуна применяют доменные печи. Для плавки цветных металлов производят внутренний нагрев с помощью токов высокой частоты.
В изложницах, изготовленных из неметаллических материалов, находятся цветные металлы в твердом состоянии. Вокруг них создают переменное магнитное поле СВЧ. В результате кристаллические решетки начинают расшатываться. Молекулы вещества приходят в движение, что вызывает разогрев внутри всей массы.
При необходимости плавки небольшого количества легкоплавких металлов используют муфельные печи. В них температура поднимается до 1000…1200 ⁰С, что достаточно для плавки цветных металлов.
Черные металлы расплавляют в конвекторах, мартенах и индукционных печах. Процесс идет с добавлением легирующих компонентов, улучшающих качество металла.
Сложнее всего проводить работу с тугоплавкими металлами. Проблема в том, что нужно использовать материалы, имеющие температуру более высокую, чем температура плавления самого металла. В настоящее время авиационная промышленность рассматривает использование в качестве конструкционного материала Титан (Ti). При высокой скорости полета в атмосфере происходит разогрев обшивки. Поэтому нужна замена алюминию и его сплавам (AL).
Максимальная температура плавления этого довольного легкого металла привлекает конструкторов. Поэтому технологи разрабатывают технологические процессы и оборудование, чтобы производить детали из титана и его сплавов.
Применение вольфрама
Этот металл обладает сравнительно высокой ценой и тяжело обрабатывается механическим способом, поэтому применяют его там, где невозможно заменить другими, сходными по свойствам материалами. Вольфрам прекрасно выдерживает высокие температуры, имеет значительную прочность, наделен твердостью, упругостью и тугоплавкостью, поэтому находит широкое использование во многих областях промышленности:
- Металлургической. Она является основным потребителем вольфрама, который идет на производство высокого качества легированных сталей.
- Электротехнической. Температура плавления самого тугоплавкого металла составляет почти 3400 °C. Тугоплавкость металла позволяет применять его для производства нитей накаливания, крючков в осветительных и электронных лампах, электродов, рентгеновских трубок, электрических контактов.

- Машиностроительной. Благодаря повышенной прочности сталей, содержащих вольфрам, изготавливают цельнокованые роторы, зубчатые колеса, коленчатые валы, шатуны.
- Авиационной. Какой самый тугоплавкий металл используют для получения твердых и жаропрочных сплавов, из которых делают детали авиационных двигателей, электровакуумных приборов, нити накаливания? Ответ прост – это вольфрам.
- Космической. Из стали, содержащей вольфрам, производят реактивные сопла, отдельные элементы для реактивных двигателей.
- Военной. Высокая плотность металла позволяет изготавливать бронебойные снаряды, пули, броневую защиту торпед, снарядов и танков, гранаты.
- Химической. Стойкая вольфрамовая проволока против кислот и щелочей используется для сеток к фильтрам. С помощью вольфрама меняют скорость химических реакций.
- Текстильной. Вольфрамовая кислота используется как краситель для тканей, а вольфрамит натрия применяют для производства кожи, шелка, водоустойчивых и огнестойких тканей.
Приведенный перечень использования вольфрама в разных областях индустрии указывает на высокую ценность этого металла.
СВОЙСТВА
Железная руда
В чистом виде при нормальных условиях это твердое вещество. Оно обладает серебристо-серым цветом и ярко выраженным металлическим блеском. Механические свойства железа включают в себя уровень твердости по шкале Мооса. Она равна четырем (средняя). Железо обладает хорошей электропроводностью и теплопроводностью. Последнюю особенность можно ощутить, дотронувшись до железного предмета в холодном помещении. Так как этот материал быстро проводит тепло, он за короткий промежуток времени забирает большую его часть из вашей кожи, и поэтому вы ощущаете холод. Дотронувшись, к примеру, до дерева, можно отметить, что его теплопроводность намного ниже. Физические свойства железа – это и его температуры плавления и кипения. Первая составляет 1539 градусов по шкале Цельсия, вторая – 2860 градусов по Цельсию. Можно сделать вывод, что характерные свойства железа – хорошая пластичность и легкоплавкость. Но и это еще далеко не все. Также в физические свойства железа входит и его ферромагнитность. Что это такое? Железо, магнитные свойства которого мы можем наблюдать на практических примерах каждый день, – единственный металл, обладающий такой уникальной отличительной чертой. Это объясняется тем, что данный материал способен намагничиваться под действием магнитного поля. А по прекращении действия последнего железо, магнитные свойства которого только что сформировались, еще надолго само остается магнитом. Такой феномен можно объяснить тем, что в структуре данного металла присутствует множество свободных электронов, которые способны передвигаться.
Когда было открыто
История знакомства человека с железом начинается с Космоса. Судя по древним (например, древнеегипетским) названиям элемента, это было метеоритное железо. Хеттские тексты упоминают о нем как об «упавшем с неба».
Человек использует металл 6 тысяч лет.
Железные изделия завоевывали мир. Металлу посвящены стихи Гомеровой «Илиады», его упоминают Аристотель и Страбон.
Небесным происхождением обусловлено античное наименование железа: «сидер» («звездный»).
Ученые исследуют потенциал металла постоянно. Так, в 1868 году русский ученый Д. К. Чернов открыл кристаллические модификации вещества.
Черные металлы
Материалы, относящиеся к этой группе, обладают одинаковыми свойствами: внушительной плотностью, большой температурой плавления и темно-серой окраской. К первой большой группе черных металлов принадлежат следующие:
- Железные – кобальт, марганец, никель, железо. Применяются в качестве основы или добавок к сплавам.
- Тугоплавкие – хром, вольфрам, молибден, титан. Все они имеют температуру плавления, превышающую уровень, при котором плавится железо. Используются как основа или добавка для получения легированных сталей.
- Урановые – актиноиды и металлы, полученные в результате синтеза. Большое применение находят в атомной энергетике.
- Редкоземельные – неодим, церий, лантан. Все металлы обладают родственными химическими свойствами, но совершенно разными физическими параметрами. Находят свое применение как присадки к сплавам.
- Щелочноземельные – кальций, натрий, литий. В свободном виде практического применения не имеют.
Состав, свойства и маркировка
По объёму потребления основным из ферросплавов является ферросилиций. Он содержит кремний, который используется для удаления кислорода из расплава. В процессе раскисления используется высокое сродство кремния к кислороду. Операция раскисления кремнием становится более эффективной, когда в ферросилиции присутствует марганец, образующий сложные силикаты. Эти силикаты надёжно связывают кислород, улучшая качество готовой продукции.

Ферросилиций получают путем восстановления кремнезема или песка с помощью кокса в присутствии железа. Материал обладает хорошей стойкостью к истиранию, хорошей стойкостью к коррозии, высоким удельным весом и высоким магнетизмом. Температура плавления и плотность ферросилиция зависят от содержания в нем кремния, и он доступен по невысокой цене.
Химический состав ферросилиция:
-
кремний – 74…78%
-
железо – не менее 21…22;
-
алюминий – не более 0,50.
В виде примесей/добавок присутствуют также углерод, марганец, сера и фосфор.
Ферросилиций – сплав железа с углеродом – обладает следующими физическими свойствами:
-
Плотность, г/см3 – 3,2.
-
Температура плавления, 0С – 1200…1250.
-
Температура кипения, 0С – 2355.
Ферросилиций отечественного производства выпускается по техническим требованиям ГОСТ 1415-93 и маркируется ФСХХ, где последние два знака – цифры, означающие процент кремния (например, ферросилиций ФС75 содержит около 75% кремния).
Сплавы системы «железо-медь» являются лигатурами – веществами, применяемыми с целью измельчения зерна, модификации или отверждения основного сплава. Применение лигатур повышает экономичность выплавки. В химический состав входит от 10 до 50 % железа, остальное приходится на медь. Около 1 % составляют примеси и добавки.

Железоникелевые и железокобальтовые сплавы обеспечивают снижение потерь в магнитопроводах, а также снижают чувствительность деталей к атмосферной коррозии. Некоторые из них обладают эффектом памяти.
Наиболее широкий диапазон магнитных свойств и чётко выраженную структуру демонстрируют сплавы никель-железо с процентным содержанием никеля 35…80%. Изменение состава достигается выбором температуры отжига и подходящей высокой скоростью охлаждения.
Общее название таких материалов – пермаллой. В отечественной практике сплавы на основе железа — пермаллои производят по ГОСТ 10160-62.
Согласно этому стандарту выпускаются пермаллои следующих групп:
-
Нелегированные (45Н, 50Н, цифры обозначают процент никеля).
-
Имеющие прямоугольную петлю гистерезиса. Маркировка — 50НП, 65НП, 34НКМП (буква П означает «прямоугольная петля», в составе последнего сплава присутствуют также молибден и кобальт.
-
Дополнительно легированные хромом и медью, иногда называемые элинварами (50ХНС, 78ХНД).
Особо следует выделить инвар (маркировка 36Н) – железоникелевый прецизионный сплав с минимальным значением коэффициента теплового расширения. Маркировка и технические требования соответствуют положениям ГОСТ 10160-62.

Сплавы железа с титаном (а также железа с титаном и алюминием, в небольших количествах присутствуют также марганец) характеризуются малой плотностью и большой прочностью. Известно, что такие свойствам сплавы обязаны особым формулам интерметаллидных соединений, которые имеются в структуре. Выпускаются в США.
Таблицы свойств металлов
Таблица «Свойства металлов: Чугун, Литая сталь, Сталь»
- Предел прочности на растяжение
- Предел текучести (или Rp 0,2);
- Относительное удлинение образца при разрыве;
- Предел прочности на изгиб;
- Предел прочности на изгиб приведен для образца из литой стали;
- Предел усталости всех типов чугуна, зависит массы и сечения образца;
- Модуль упругости;
- Для серого чугуна модуль упругости уменьшается с увеличением напряжения растяжения и остается практически постоянным с увеличением напряжения сжатия.
Таблица «Свойства пружинной стали»
Пример HTML-страницы
- Предел прочности на растяжение,
- Относительное уменьшение поперечного сечения образца при разрыве,
- Предел прочности на изгиб;
- Предел прочности при знакопеременном циклическом нагружении при N ⩾ 107,
- Максимальное напряжение при температуре 30°С и относительном удлинении 1 2% в течение 10 ч; для более высоких температур см. раздел «Способы соединения деталей»;
- 480 Н/мм2 для нагартованных пружин;
- Приблизительно на 40% больше для нагартованных пружин
Таблица «Свойства цветных металлов»
- Модуль упругости, справочные данные;
- Предел прочности на растяжение;
- Предел текучести, соответствующий пластической деформации 0,2%;
- Предел прочности на изгиб;
- Наибольшая величина;
- Для отдельных образцов
Таблица «Свойства легких сплавов»
- Предел прочности на растяжение;
- Предел текучести, соответствующий пластической деформации 0,2%;
- Предел прочности на изгиб;
- Наибольшая величина;
- Показатели прочности приведены для образцов и для отливок;
- Показатели предела прочности на изгиб приведены для случая плоского нагружения
Таблица «Металлокерамические материалы (PM)1) для подшипников скольжения»
- В соответствии со стандартом DIN 30 910,1990 г. издания;
- Применительно к подшипнику 10/16 г 10;
- Углерод содержится, главным образом, в виде свободного графита;
- Углерод содержится только в виде свободного графита
Классификация металлов по температуре плавления
В физике переход твердого тела в жидкое состояние характерен только для веществ кристаллической структуры. Температуру плавления металлов чаще обозначают диапазоном значений, для сплавов точно определить нагрев до пограничного фазового состояния сложно. Для чистых элементов каждый градус имеет значение, особенно, если это легкоплавкие элементы,
значения не имеет. Сводная таблица показателей t обычно делится на 3 группы. Помимо легкоплавких элементов, которые максимально нагревают до +600°С, указывают тугоплавкие, выдерживающие нагрев свыше +1600°С, и среднеплавкие. В этой группе сплавы, образующие ванну расплава при температуре от +600 до 1600°С.
Типы сплавов
В зависимости от интенсивности нагрева, требуемого для перехода металла из одного состояния в другое, сплавы разделяют на несколько видов.
Легкоплавкие. Их обработка может производиться даже без специального оборудования. Температура плавления стали в градусах Цельсия составляет 600. К числу легкоплавких металлов относятся свинец, олово и цинк.
Особого внимания заслуживает ртуть, способная переходить в жидкое состояние при -39°С.
Среднеплавкие. Температура плавления сталей находится в пределах 600°С-1600°С. К этой категории относятся алюминий, медь, олово, некоторые виды нержавейки и различные сплавы с небольшим содержанием хрома. Среднеплавкие соединения получили наибольшее распространение в промышленности и в быту.
Тугоплавкие. Соединения, входящие в данную категорию, способны переходить из твердого состояния в жидкое при нагреве свыше 1600°С. Это высоколегированные металлы, в состав которых входят вольфрам, титан и хром. Благодаря этим добавкам металл приобретает повышенную прочность, устойчивость к коррозии и химическим воздействиям. В частности, к тугоплавким сплавам относится нержавейка.
При наиболее низких температурных показателях плавятся щелочные металлы. Соответственно, для перехода в жидкое состояние не щелочных металлов температурный диапазон значительно увеличивается.
Градус кипения
В процессе нагрева материала важно не достичь его кипения, при котором из жидкого состояния он переходит в газообразное. Поэтому градус кипения является не менее важным технологическим показателем
Градус кипения, как правило, вдвое выше градуса, при котором материалы расплавляются, и определяется при нормальном атмосферном давлении. При увеличении давления увеличивается и интенсивность нагрева. При уменьшении давления показатели уменьшаются.
Особенности углеродистой стали
Углеродистые соединения являются основным видом продукции, производимой на металлургических комбинатах. Кроме железа, в их состав входит углерод. Его концентрация не должна превышать 2,14%. В них присутствует небольшое количество примесей и легирующих компонентов в виде марганца, кремния и магния. Такие добавки позволяют улучшить их физические и химические показатели.
В зависимости от концентрации углерода углеродистые соединения делятся на следующие виды:
- низкоуглеродистые (содержание углерода не превышает 0,29%);
- среднеуглеродистые (до 0,6%);
- высокоуглеродистые (более 0,6%).
Углеродистые соединения используются в различных промышленных отраслях. В зависимости от сферы применения в них добавляются легирующие компоненты, позволяющие достичь специфических свойств, включая жаропрочность, коррозийную стойкость и пр. По этим критериям они подразделяются на следующие категории:
- конструкционные;
- инструментальные.
В инструментальные добавляется марганец, позволяющий значительно повысить качество металла. Температура плавления углеродистой стали составляет 1535°С.
Особенности легированной стали
В состав легированных соединений вводят дополнительные компоненты. В определенных количествах они придают им требуемые свойства. В зависимости от концентрации таких элементов они подразделяются на следующие виды:
- низколегированные (с концентрацией 2,5%);
- среднелегированные (до 10%);
- высоколегированные (свыше 10%).
За счет добавления дополнительных компонентов удается повысить прочность, коррозийную стойкость и улучшить другие характеристики. В качестве легирующих компонентов выступают хром, медь, никель, азот, ванадий и пр. Температура плавления легированной стали колеблется в пределах 1400°С-1480°С.
Особенности нержавейки
Нержавейка – это сплав, устойчивый к сухой и влажной коррозии, и невосприимчивый к воздействию агрессивных веществ. Чтобы придать ему необходимые свойства, в металл добавляются различные легирующие компоненты в виде хрома, никеля, магния, титана и пр. Температура плавления нержавеющей стали по Цельсию составляет 1350-1500 градусов.
Ниже представлена таблица, в которой указана температура плавления жаропрочной нержавеющей стали наиболее популярных марок.
| Марка | t°С |
| 12Х18Г9 | 1410 |
| Х20Н35 | 1410 |
| 12Х18Н9Т | 1425 |
| Х25С3Н | 1480 |
| 15Х25Т | 1500 |
Особенности инструментальной стали
Этот материал предназначен исключительно для изготовления инструментов. От конструкционного он отличается увеличенным содержанием углерода в количестве более 0,7%. Такие соединения в основном используются в машиностроении для обработки чермета и цветмета. Температура плавления нержавеющей стали, предназначенной для изготовления инструмента, составляет 1500°С.
Использование сульфата железа в строительстве
Это химическое вещество исстари применяли для увеличения долговременности деревянных построек.
Начиная с античных греков люди искали материалы, которые помогали бы защитить древесину домов от гниения. Они покрывали их растительными маслами, затем различными красками и лаками. Эффект, в лучшем случае, был не долговременным. Краски и лаки отшелушивались и в этих местах быстро начинали развиваться процессы гниения.
Много более эффективным оказался путь уничтожения бактерий и грибков, разрушающих древесину при помощи различных химических веществ. Сегодня такой метод называется биоцидным. В его основе – пропитка древесины импрегнантами (антисептическими растворами) Среди наиболее эффективных импрегнантов — железный купорос.
Для защиты древесины раствор железного купороса:
- наносят на деревянные поверхности малярными кистями;
- наносят на деревянные детали при помощи распыления распылителем;
- деревянные конструкции погружают в раствор сульфата железа полностью, при этом для повышения эффективности производят их прогревание в растворе.
Еще больший позитивный эффект дает промышленное обрабатывание сернокислым железом деревянных конструкций. Его выполняют одним из ниже приведенных методов:
- пропитывают раствором сульфата железа в автоклавах;
- при помощи диффузионной пропитки, в ходе которой на деревянные детали наносят слой пастообразного материала, который содержит сернокислое железо, постепенно поникающее в материал полностью пропитывая его структуру.
В сельских местностях скандинавских стран и по сегодня применяют старинный специальный состав для окрашивания домов и заборов с целью их защиты от гниения на основе сульфата железа. В состав входят:
- вода 9 литров;
- купорос железный – 1,56 килограмма;
- мука – 0,72 килограмма;
- известковый пигмент сухой – 1,56 килограмма;
- соль – 0,36 килограмма.
В муку постепенно вводят 1/3 части воды и размешивают до получения клейстера, который процеживают и затем нагревают постоянно тщательно размешивая, а затем вводят соль, известковый пигмент и железный купорос – после их полного растворения добавляют остаток воды, предварительно нагрев его.
В случае желания придания краске какого-либо цвета – в неё добавляют соответствующие пигменты. Краску на деревянные поверхности наносят без грунтовки и в два слоя. Расход краски при этом составляет 0,3 килограмма на квадратный метр. Минимальный срок эксплуатации таких поверхностей при атмосферных условиях Норвегии, северных областей Финляндии – двадцать лет.
К достоинствам пропиток на основе сульфата железа строители относят его хорошую водорастворимость (в холодной воде можно приготовить 25% раствор, в горячей – 55%), а также то, что такие растворы не корродируют железные детали.
В России был изобретен и забинтован метод изготовления древесно-волокнистых и древесно-стружечных плит для строительной и мебельной промышленности из древесных материалов, содержащих целлюлозу и лигнин путем их поэтапной обработки. На одном из этапов основным элементом сложной технологии выступает такой модифицирующий агент, как сульфат железа, который вводят в разогретую паром древесную массу при t=190°C, а затем прессуют в плиты при t=190°C.
Поскольку в данном методе не используются вещества фенольной природы – получаются экологически безопасные плиты повышенной прочности, не подверженные процессам гниения и не выделяющие при эксплуатации формальдегидов. Такие плиты также просты в обработке, влагоустойчивы, мало горючи.
Модифицирующая добавка из сульфата железа одновременно значительно повышает прочность плиточного материала, укорачивает время, нужное для изготовления плит. В строительной промышленности сульфат железа применяют и при изготовлении клинкерных смесей, сухих штукатурок, цементов для удаления ионов шестивалентного хрома.
Добыча полезных ископаемых
Руд, в которых присутствует железо, существует несколько. Однако, в качестве сырья для производства железа в промышленности используют в основном следующие:
- магнезитовую руду;
- гетитовую руду;
- гематитовую руду.
А также часто встречаются такие разновидности руды:
- леллингит;
- сидерит;
- марказит;
- ильменит;
- ярозит.
Существует еще минерал под названием мелантерит. Его используют преимущественно в фармацевтической промышленности. Из себя он представляет зелёного цвета хрупкие кристаллы, в которых присутствует стеклянный блеск. Из него производят лекарственные препараты, в составе которых имеется ферум.
Основным месторождением этого металла является Южная Америка, а именно Бразилия.















![4. классификация сплавов. железо и его сплавы. материаловедение: конспект лекций [litres]](http://takorest.ru/wp-content/uploads/6/f/e/6fe7fc9b82397b9897d40331be5315ed.png)














